题目内容
13.判断正误,并说明理由:①1mol NaCl和1mol HCl含有相同粒子数目;
②1mol O2的质量与它的相对分子质量相等
③氖气的摩尔质量(单位:g/mol)在数值上等于它的相对原子质量
④2mol水的摩尔质量是1mol水的摩尔质量的两倍.
分析 ①NaCl是钠离子和氯离子构成的,HCl是分子构成的;
②质量与相对分子质量的单位是不一样的;
③摩尔质量(单位:g/mol)在数值上等于它的相对原子质量;
④摩尔质量在数值上等于它的相对原子质量,和物质的物质的量多少无关.
解答 解:①NaCl是钠离子和氯离子构成的,HCl是分子构成的,1mol NaCl含有2mol离子,1mol HCl含有1mol分子,1mol NaCl和1mol HCl含有粒子数目不一样,故错误;
答:错误; 1mol NaCl含有2mol离子,1mol HCl含有1mol分子,1mol NaCl和1mol HCl含有粒子数目不一样;
②质量的单位是g,相对分子质量的单位是1,1mol O2的质量与它的相对分子质量不一样,
答:错误;1mol O2的质量与它的相对分子质量不相等,前者有单位,后者没有;
③摩尔质量(单位:g/mol)在数值上等于它的相对原子质量,答:正确;
④摩尔质量在数值上等于它的相对原子质量,和物质的物质的量多少无关,
答:错误;摩尔质量和物质的物质的量多少无关,2mol水的摩尔质量和1mol水的摩尔质量是相等的.
点评 本题考查学生有关物质的摩尔质量以及相对原子(分子)质量之间的关系,注意单位之间的关系是关键,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.相同浓度溶液中某些物质量之间的关系:
现有两种溶液:①1mol•L-1KCl溶液;②1mol•L-1BaCl2溶液,请用“相同”或“不同”填写表格.
现有两种溶液:①1mol•L-1KCl溶液;②1mol•L-1BaCl2溶液,请用“相同”或“不同”填写表格.
| 取不同体积的KCl溶液 | 取相同体积的两种溶液 | |
| c(溶质) | 相同 | 相同 |
| ρ(溶质) | 相同 | 不同 |
| n(溶质) | 不同 | 相同 |
| m(溶质) | 不同 | 不同 |
1.已知在相同温度和压强下,任何气体的分子数之比等于体积比.现有CO、O2、CO2混合气体9mL,点燃爆炸后,恢复到原来状况时,体积减少1mL,再通过足量NaOH溶液体积又减少5mL,则原混合气体中CO、O2、CO2的体积比可能是( )
| A. | 1:3:5 | B. | 5:1:3 | C. | 3:1:5 | D. | 2:4:3 |
8.在标准状况下,wL氮气含有x个N原子,用ω和x表示阿伏加德罗常数为( )
| A. | wx mol-1 | B. | 22.4x mol-1 | C. | $\frac{22.4x}{ω}$mol-1 | D. | $\frac{11.2x}{ω}$mol-1 |
12.据报道,上海某医院正在研究用放射性的一种碘${\;}_{53}^{125}I$治疗肿瘤.下列有关${\;}_{53}^{125}I$叙述错误的是( )
| A. | ${\;}_{53}^{125}I$是碘的一种核素 | |
| B. | ${\;}_{53}^{125}I$核内的中子数与核外电子数之差为19 | |
| C. | ${\;}_{53}^{125}I$质量数为l25 | |
| D. | ${\;}_{53}^{125}I$是一种新发现的元素 |
9.NA代表阿伏加德罗常数值,下列说法正确的是( )
| A. | 78gNa2O2所含有的离子数为3NA | |
| B. | 1mol甲基中含有电子数为10NA | |
| C. | 7.1g氯气与足量NaOH溶液反应转移的电子数为0.2NA | |
| D. | 1molC10H22分子中共价键总数为22NA |
7.原子序数依次增大的元素a、b、c、d,它们的最外层电子数分别为1、6、7、1.a-的电子层结构与氦相同,b和c的次外层有8个电子,c-和d+的电子层结构相同.下列叙述错误的是( )
| A. | a和其他3种元素均能形成共价化合物 | |
| B. | 元素的非金属性次序为c>b>a | |
| C. | d和其他3种元素均能形成离子化合物 | |
| D. | 元素a、b、c各自最高和最低化合价的代数和分别为0、4、6 |
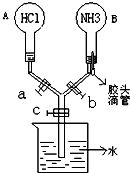 如图所示的装置,实验前a、b、c活塞均关闭.
如图所示的装置,实验前a、b、c活塞均关闭.