题目内容
3.下列排列顺序正确的是( )①固体热稳定性:Na2CO3>CaCO3>NaHCO3
②微粒半径:F->Na+>Mg2+>S2-
③燃烧热:S(气体)>S(液体)>S(固体)
④物质的熔点:植物油>动物油.
| A. | ①③④ | B. | ①③ | C. | ①②③④ | D. | ②③④ |
分析 ①NaHCO3加热分解,CaCO3高温分解,Na2CO3不分解;
②电子层数越多,半径越大,核外电子排布相同时,核电核数越大,半径越小;
③物质的能量越高,燃烧热越大;
④动物油常温下为固态,植物油常温下为液态.
解答 解:①NaHCO3加热分解,CaCO3高温分解,Na2CO3不分解,所以固体热稳定性顺序为Na2CO3>CaCO3>NaHCO3,故正确;
②F-、Na+、Mg2+、S2-中,S2-核外有3个电子层,其它离子核外有2的电子层,核外电子层数越多,半径越大;F-、Na+、Mg2+核外电子排布相同,核电核数越大,半径越小,正确顺序为:S2->F->Na+>Mg2+,故错误;
③不同聚集状态的物质能量不同,能量大小顺序为:气态>液态>固态,物质的能量越高,燃烧热越大,故正确;
④物油常温下为固态,植物油常温下为液态,熔点:动物油>植物油,故错误;
综上所述正确的为①③,故选B.
点评 本题考查微粒半径大小比较、燃烧热、溶质熔沸点高低判断等知识点,综合性较强,离子半径与电子层数有关,知道物质聚集状态与燃烧热的关系,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.下列各组物质的性质比较,正确的是( )
| A. | 还原性:F-<Cl-<Br-<I- | B. | 碱性:NaOH<Mg(OH)2<Al(OH)3 | ||
| C. | 氢化物稳定性:H2S>HF>H2O | D. | 酸性:HClO4>H3PO4>H2SO4 |
14.短周期元素Q、W、X、Y、Z原子序数依次增大,X元素的焰色反应呈黄色,Q原子的最外层电子数是其内层电子数的2倍.W、Z原子的最外层电子数相同,Z元素的核电荷数是W的2倍,Y是地壳中含量最多的金属元索.下列说法正确的是( )
| A. | 原子半径的大小顺序:rX>rY>rW>rQ | |
| B. | 工业上常用电解的方法制备X,Y的单质 | |
| C. | 元素Q和Z能形成QZ2的共价化合物为原子晶体 | |
| D. | 元素X、Y的最高价氧化物对应水化物之间不能反应 |
11.阿司匹林是常见的解热镇痛药,其结构简式如图所示,下列有关说法正确的是( )


| A. | 阿司匹林的分子式为C9H10O4 | B. | 阿司匹林属于有机高分子化合物 | ||
| C. | 1mol阿司匹林最多能与5molH2加成 | D. | 阿司匹林具有酸性,能与NaOH反应 |
18. “茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )
“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )
 “茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )
“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )| A. | 分子中所有的原子共面 | B. | 1molEGC与3molNaOH恰好完全反应 | ||
| C. | 它具有酯的性质 | D. | 遇FeCl3溶液发生显色反应 |
8.L-多巴是一种有机物,它可用于帕金森综合症的治疗,其结构简式如图所示,这种药物的研制是基于获得2000年诺贝尔生理学和医学奖、2001年诺贝尔化学奖的研究成果.下列关于 L-多巴酸性质的叙述正确的是( )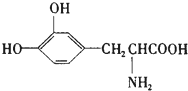

| A. | 只能与碱反应,不能与酸反应 | B. | 1mol该物质最多可与4molNaOH反应 | ||
| C. | 该物质不能使酸性KMnO4褪色 | D. | 1mol该物质最多可与1molHBr反应 |
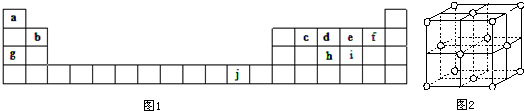
 ,ci2与ce2比较,沸点较高的是CS2(写分子式).
,ci2与ce2比较,沸点较高的是CS2(写分子式).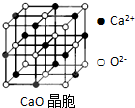 工业上,可以由下列反应合成三聚氰胺:
工业上,可以由下列反应合成三聚氰胺: .其中氮原子的杂化方式有sp2、sp3.
.其中氮原子的杂化方式有sp2、sp3.