题目内容
20.在25℃,101k P的条件下,5.2g C2H2完全燃烧生成CO2和H2O(l)时放出259.92kJ热量.表示上述反应的热化学方程式正确的是( )| A. | 1/5C2H2(g)+1/2O2(g)=2/5CO2(g)+1/5H2O(l)△H=+259.92 kJ/mol | |
| B. | 0.2C2H2(g)+0.5O2(g)=0.4CO2(g)+0.2H2O(l)△H=-259.92 kJ/mol | |
| C. | 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H=+2599.2 kJ/mol | |
| D. | 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(g)△H=-2599.2 kJ/mol |
分析 根据5.2g 即$\frac{5.2g}{26g/mol}$=0.2mol C2H2完全燃烧生成CO2和H2O(l)时放出259.92kJ热量,则反应的热化学方程式为0.2C2H2(g)+0.5O2(g)=0.4CO2(g)+0.2H2O(l)△H=-259.92 kJ/mol,结合热化学方程式中反应热与物质的物质的量成正比来判断.
解答 解:A、反应是放热的,所以焓变是负数,故A错误;
B、5.2g 即$\frac{5.2g}{26g/mol}$=0.2mol C2H2完全燃烧生成CO2和H2O(l)时放出259.92kJ热量,则0.2C2H2(g)+0.5O2(g)=0.4CO2(g)+0.2H2O(l)△H=-259.92 kJ/mol,故B正确;
C、反应是放热的,所以焓变是负数,故C错误;
D、5.2g 即$\frac{5.2g}{26g/mol}$=0.2mol C2H2完全燃烧生成CO2和H2O(l)时放出259.92kJ热量,则2mol C2H2完全燃烧生成CO2和H2O(l)时放出2599.2kJ热量,2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H═-2599.2 kJ/mol,而不是生成气态水,故D错误.
故选B.
点评 本题考查热化学方程式,题目难度不大,做题时要注意热化学方程式中反应热与物质的物质的量成正比以及反应热的符号是否正确.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
10.对于SO2和CO2的说法中正确的是( )
| A. | 都是直线形结构 | B. | 中心原子都采用SP杂化轨道 | ||
| C. | SO2为V形结构,CO2为直线形结构 | D. | S原子和C原子上都没有孤对电子 |
11.由2-氯丙烷制得少量的CH2OHCHOHCH3 需要经过下列几步反应( )
| A. | 加成→消去→取代 | B. | 消去→加成→水解 | C. | 取代→消去→加成 | D. | 消去→加成→消去 |
15.氰酸铵(NH4CNO)与尿素[CO(NH2)2]( )
| A. | 互为同系物 | B. | 互为同分异构体 | C. | 都是共价化合物 | D. | 都是有机化合物 |
5.炼铁高炉中冶炼铁的反应为:Fe2O3(s)+3CO(g)$\frac{\underline{\;高温\;}}{\;}$2Fe(s)+3CO2(g),下列说法正确的是( )

| A. | 升高温度,反应速率减慢 | |
| B. | 当反应达到化学平衡时,υ(正)=υ(逆)=0 | |
| C. | 提高炼铁高炉的高度可减少尾气中CO的浓度 | |
| D. | 某温度下达到平衡时,CO的体积分数基本不变 |
9.0.1mol•L-1下列溶液与0.2mol•L-1氢氧化钡溶液等体积混合,产生沉淀质量最大的是( )
| A. | KAl(SO4)2 | B. | NH4Al(SO4)2 | C. | (NH4)2Fe(SO4)2 | D. | NH4Fe(SO4)2 |
17.下表实验中“操作及现象”与“给定溶液”的性质不对应的是( )
| 选项 | 溶液 | 操作及现象 |
| A | Ca(OH)2溶液 | 通入CO2,溶液变浑浊.继续通CO2至过量,浑浊消失.再加入足量NaOH溶液,又变浑浊. |
| B | 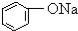 溶液 溶液 | 通入CO2,溶液变浑浊.继续通CO2至过量,浑浊消失. |
| C | Ca(ClO)2溶液 | 通入CO2,溶液没有明显变化.再滴入品红溶液,红色褪去. |
| D | CaCl2溶液 | 通入CO2,溶液没有明显变化.若同时通入CO2和NH3,则溶液变浑浊. |
| A. | A | B. | B | C. | C | D. | D |
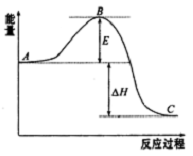 2SO2(g)+O2 (g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1molSO3(g)的△H=-99kJ•mol-1
2SO2(g)+O2 (g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1molSO3(g)的△H=-99kJ•mol-1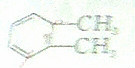 )加氢产物1,2-二甲基环乙烷(
)加氢产物1,2-二甲基环乙烷( )的一氯代产物有(不考虑立体异构)( )
)的一氯代产物有(不考虑立体异构)( )