题目内容
17.下表实验中“操作及现象”与“给定溶液”的性质不对应的是( )| 选项 | 溶液 | 操作及现象 |
| A | Ca(OH)2溶液 | 通入CO2,溶液变浑浊.继续通CO2至过量,浑浊消失.再加入足量NaOH溶液,又变浑浊. |
| B | 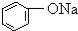 溶液 溶液 | 通入CO2,溶液变浑浊.继续通CO2至过量,浑浊消失. |
| C | Ca(ClO)2溶液 | 通入CO2,溶液没有明显变化.再滴入品红溶液,红色褪去. |
| D | CaCl2溶液 | 通入CO2,溶液没有明显变化.若同时通入CO2和NH3,则溶液变浑浊. |
| A. | A | B. | B | C. | C | D. | D |
分析 A.根据氢氧化钙和碳酸钙以及碳酸氢钙的化学性质来解答;
B.苯酚高于65℃与水混溶,室温时溶解度较小,碳酸的酸性大于苯酚的酸性,苯酚的酸性强于碳酸氢根离子,所以苯酚钠和二氧化碳和水反应生成碳酸氢钠和苯酚;
C.碳酸酸性强于次氯酸,碳酸钙在过量二氧化碳存在下会转化为碳酸氢钙,次氯酸具有强氧化性,可使品红褪色;
D.盐酸酸性强于碳酸,CaCl2溶液与CO2不反应,CaCl2溶液与氨气、二氧化碳反应生成碳酸钙沉淀.
解答 解:A.氢氧化钙中通二氧化碳会生成碳酸钙沉淀和水,继续通CO2至过量,碳酸钙和二氧化碳和水反应,碳酸钙沉淀再转化为易溶于水的碳酸氢钙,碳酸氢钙和氢氧化钠反应会生成碳酸钙沉淀,又变浑浊,故A正确;
B.65℃以上苯酚易溶于水,室温下苯酚的溶解度较小,苯酚钠和二氧化碳反应生成难溶性的苯酚和碳酸氢钠,溶液变浑浊,继续通CO2至过量,苯酚、碳酸氢钠和过量的二氧化碳不反应,溶液仍浑浊,故B错误;
C.向Ca(ClO)2溶液中通入二氧化碳,会生成碳酸钙和次氯酸,碳酸钙在过量二氧化碳存在下会转化为碳酸氢钙,沉淀消失,次氯酸具有强氧化性,可使品红褪色,故C正确;
D.CaCl2溶液与CO2不反应,若同时通入CO2和NH3,在碱性条件下,CaCl2溶液与氨气、二氧化碳反应生成碳酸钙沉淀,溶液变浑浊,故D正确.
故选B.
点评 本题考查物质的鉴别和检验,题目难度中等,解答本题的关键是把握相关物质的性质,易错点为B,注意65℃以上苯酚易溶于水,苯酚的酸性强于碳酸氢根离子,苯酚钠和二氧化碳和水反应生成碳酸氢钠和苯酚.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
20.在25℃,101k P的条件下,5.2g C2H2完全燃烧生成CO2和H2O(l)时放出259.92kJ热量.表示上述反应的热化学方程式正确的是( )
| A. | 1/5C2H2(g)+1/2O2(g)=2/5CO2(g)+1/5H2O(l)△H=+259.92 kJ/mol | |
| B. | 0.2C2H2(g)+0.5O2(g)=0.4CO2(g)+0.2H2O(l)△H=-259.92 kJ/mol | |
| C. | 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H=+2599.2 kJ/mol | |
| D. | 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(g)△H=-2599.2 kJ/mol |
8.某学生小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将酸式滴定管用蒸馏水洗净,用标准盐酸(0.1000mol/L)溶液润洗2遍,注入标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0”或“0”以下刻度;将锥形瓶用蒸馏水洗净后,也用该盐酸溶液润洗2遍;从酸式滴定管中放出20.00mL溶液到锥形瓶中.
②将碱式滴定管用蒸馏水洗净,用待测NaOH溶液润洗2遍,调节滴定管尖嘴部分充满溶液,并使液面处于“0”或“0”以下刻度.
③向锥形瓶中滴入酚酞作指示剂,进行滴定并用pH计记录pH变化.滴定至指示剂刚好变色,且并不马上恢复原来颜色为止,记录碱式滴定管液面读数.再继续滴定,并记录pH至无明显变化为止.
重复上述取样、滴定工作2次,记录每次实验所用碱溶液体积.
回答下列问题:
(1)图1中有2根滴定管,其中b(选填“a”、“b”)是酸式滴定管.
(2)滴定过程中,边滴边摇动锥形瓶,眼睛应观察a(选填“a”、“b”).
a.锥形瓶内溶液颜色的变化 b.滴定管内液面的变化
(3)该小组在步骤①中有一个明显的错误操作,由此造成测定结果偏高 (选填“偏高”、“偏低”或“无影响”).
(4)图2中该滴定过程的滴定曲线是下列的a(选填“a”、“b”).

(5)有关数据记录如下:
则该小组计算得到NaOH溶液的物质的量浓度为0.10mol/L.
①将酸式滴定管用蒸馏水洗净,用标准盐酸(0.1000mol/L)溶液润洗2遍,注入标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0”或“0”以下刻度;将锥形瓶用蒸馏水洗净后,也用该盐酸溶液润洗2遍;从酸式滴定管中放出20.00mL溶液到锥形瓶中.
②将碱式滴定管用蒸馏水洗净,用待测NaOH溶液润洗2遍,调节滴定管尖嘴部分充满溶液,并使液面处于“0”或“0”以下刻度.
③向锥形瓶中滴入酚酞作指示剂,进行滴定并用pH计记录pH变化.滴定至指示剂刚好变色,且并不马上恢复原来颜色为止,记录碱式滴定管液面读数.再继续滴定,并记录pH至无明显变化为止.
重复上述取样、滴定工作2次,记录每次实验所用碱溶液体积.
回答下列问题:
(1)图1中有2根滴定管,其中b(选填“a”、“b”)是酸式滴定管.
(2)滴定过程中,边滴边摇动锥形瓶,眼睛应观察a(选填“a”、“b”).
a.锥形瓶内溶液颜色的变化 b.滴定管内液面的变化
(3)该小组在步骤①中有一个明显的错误操作,由此造成测定结果偏高 (选填“偏高”、“偏低”或“无影响”).
(4)图2中该滴定过程的滴定曲线是下列的a(选填“a”、“b”).

(5)有关数据记录如下:
| 实验序号 | 盐酸标准液体积(mL) | 所消耗氢氧化钠标准液的体积(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.50 | 20.70 |
| 2 | 20.00 | 2.00 | 22.00 |
| 3 | 20.00 | 1.00 | 20.80 |
5.对于元素周期表,下列叙述中不正确的是( )
| A. | 在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素 | |
| B. | 在过渡元素中可以寻找制备催化剂及耐高温和耐腐蚀的元素 | |
| C. | 在金属元素区域可以寻找制备新型农药材料的元素 | |
| D. | 元素周期表是元素周期律的具体表现形式 |
2.下列物质不能通过两种单质化合得到的是( )
| A. | Cu2S | B. | FeS | C. | Fe2S3 | D. | ZnS |
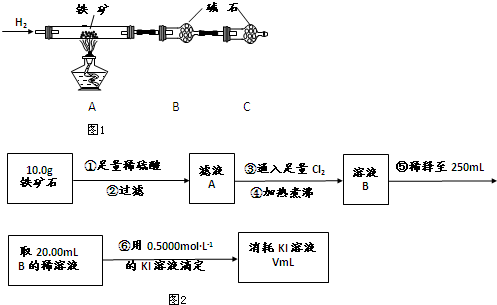
9.Na2S2O3•5H2O(俗称海波)是照相业常用的一种定影剂.工业上制得的Na2S2O3•5H2O晶体中可能含有少量的Na2SO3和Na2SO4杂质.为了测定某海波样品的成分,称取三份质量不同的该样品,分别加入相同浓度的硫酸溶液30mL,充分反应后滤出硫,微热滤液使生成的SO2全部逸出.(Na2S2O3+H2SO4γNa2SO4+SO2↑+S↓+H2O)
测得有关实验数据如下(标准状况):
(摩尔质量:Na2S2O3•5H2O 248g/mol; Na2SO3126g/mol;Na2SO4 142g/mol)
(1)计算所用硫酸溶液的物质的量浓度.
(2)分析以上实验数据,该样品中d(填写选项字母).
A.仅含有Na2S2O3•5H2O
B.含有和Na2S2O3•5H2O和Na2SO3,无Na2SO4
C.含有Na2S2O3•5H2O、Na2SO3和Na2SO4
(3)若将30.16g该样品和一定量的上述硫酸溶液混合微热.试讨论:当加入硫酸的体积(aL)在不同取值范围时,生成的S02体积(b L)的值(可用含a的关系式表示).
测得有关实验数据如下(标准状况):
| 第一份 | 第二份 | 第三份 | |
| 样品的质量/g | 7.54 | 15.08 | 35.00 |
| 二氧化硫的体积/L | 0.672 | 1.344 | 2.688 |
| 硫的质量/g | 0.8 | 1.6 | 3.2 |
(1)计算所用硫酸溶液的物质的量浓度.
(2)分析以上实验数据,该样品中d(填写选项字母).
A.仅含有Na2S2O3•5H2O
B.含有和Na2S2O3•5H2O和Na2SO3,无Na2SO4
C.含有Na2S2O3•5H2O、Na2SO3和Na2SO4
(3)若将30.16g该样品和一定量的上述硫酸溶液混合微热.试讨论:当加入硫酸的体积(aL)在不同取值范围时,生成的S02体积(b L)的值(可用含a的关系式表示).
6.下列说法正确的是( )
| A. | 二氧化锰是催化剂,能加快反应速率 | |
| B. | 温度越高,催化剂的催化效果越好 | |
| C. | 食品包装袋中的抗氧化剂就是“负催化剂”,能使氧化还原反应的速率减慢 | |
| D. | 升高温度,吸热反应和放热反应的反应速率都加快 |