题目内容
5.炼铁高炉中冶炼铁的反应为:Fe2O3(s)+3CO(g)$\frac{\underline{\;高温\;}}{\;}$2Fe(s)+3CO2(g),下列说法正确的是( )
| A. | 升高温度,反应速率减慢 | |
| B. | 当反应达到化学平衡时,υ(正)=υ(逆)=0 | |
| C. | 提高炼铁高炉的高度可减少尾气中CO的浓度 | |
| D. | 某温度下达到平衡时,CO的体积分数基本不变 |
分析 A、温度升高,化学反应速率加快;
B、当反应达到平衡时,正逆反应速率相等,但不等于零;
C、此反应特点为反应前后气体体积不变的反应,据此判断;
D、当反应达到平衡时,体系中的组成保持不变.
解答 解:A、升高温度,反应速率加快,降低温度,化学反应速率减慢,故A错误;
B、可逆反应是动态平衡,当反应达到平衡时,正逆反应速率相等,不等于零,故B错误;
C、此反应特点为反应前后气体体积不变的反应,提高炼铁高炉的高度,对平衡无影响,故C错误;
D、当反应达到平衡时,体系中的组成保持不变,所以一氧化碳与二氧化碳的物质的量之比也保持不变,故D正确;
故选D.
点评 本题主要化学平衡的特征及影响平衡移动的外界因素,难度不大,注意基础知识的运用.

练习册系列答案
相关题目
15.向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液,下列对此现象的说法正确的是( )
| A. | 反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 | |
| B. | 沉淀溶解后,将生成深蓝色的配合离子[Cu(NH3)4]2+ | |
| C. | [Cu(NH3)4]2+的空间构型为正四面体型 | |
| D. | 在[Cu(NH3)4]2+离子中,Cu2+给出孤对电子,NH3提供空轨道 |
13.下列化学用语对应正确的是( )
| A. | Cl-离子的结构示意图: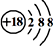 | B. | 白磷分子的比例模型: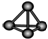 | ||
| C. | H2O2的结构式:H-O-O-H | D. | CCl4的电子式: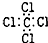 |
20.在25℃,101k P的条件下,5.2g C2H2完全燃烧生成CO2和H2O(l)时放出259.92kJ热量.表示上述反应的热化学方程式正确的是( )
| A. | 1/5C2H2(g)+1/2O2(g)=2/5CO2(g)+1/5H2O(l)△H=+259.92 kJ/mol | |
| B. | 0.2C2H2(g)+0.5O2(g)=0.4CO2(g)+0.2H2O(l)△H=-259.92 kJ/mol | |
| C. | 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H=+2599.2 kJ/mol | |
| D. | 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(g)△H=-2599.2 kJ/mol |
10.对于常温下0.1mol•L-1氨水和0.1mol•L-1醋酸,下列说法正确的是( )
| A. | 0.1mol•L-1醋酸,溶液的pH=1 | |
| B. | 0.1mol•L-1醋酸加水稀释,溶液中离子浓度都减小 | |
| C. | 0.1mol•L-1氨水溶液中:c(OH-)=c(NH${\;}_{4}^{+}$) | |
| D. | 0.1mol•L-1氨水与0.1mol•L-1 HCl溶液等体积混合所得溶液中:c(Cl-)>c(NH${\;}_{4}^{+}$)>c(H+)>c(OH-) |
2.下列物质不能通过两种单质化合得到的是( )
| A. | Cu2S | B. | FeS | C. | Fe2S3 | D. | ZnS |
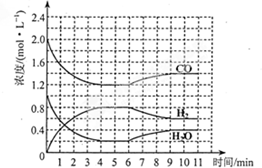 工业上和净化后的水煤气在催化剂作用下,与水蒸气发生反应制取氢气,化学方程式为:CO(g)+H2O(g)?H2(g)+CO2(g).一定条件下,将4molCO与2molH2O(g)充入体积为2L的密闭容器中,体系中各物质的深度随时间变化如图所示:
工业上和净化后的水煤气在催化剂作用下,与水蒸气发生反应制取氢气,化学方程式为:CO(g)+H2O(g)?H2(g)+CO2(g).一定条件下,将4molCO与2molH2O(g)充入体积为2L的密闭容器中,体系中各物质的深度随时间变化如图所示: