题目内容
5.下列关于乙二醇和丙三醇的说法中,不正确的是( )| A. | 乙二醇的水溶液凝固点很低,可作汽车发动机的抗冻剂 | |
| B. | 丙三醇的沸点比乙二醇的沸点高,可用于配制化妆品 | |
| C. | 这两种多元醇都易溶于水,但难溶于有机溶剂 | |
| D. | 丙三醇可以制造炸药,乙二醇是制涤纶的主要原料 |
分析 A.乙二醇的水溶液凝固点很低;
B.碳原子数越多,羟基数越多,沸点越高;
C.乙二醇和丙三醇易溶于乙醇,也易溶于水;
D.硝酸甘油是炸药;涤纶是以对苯二甲酸或对苯二甲酸二甲酯和乙二醇为原料经酯化或酯交换和缩聚反应而制得的成纤高聚物-聚对苯二甲酸乙二醇酯.
解答 解:A.乙二醇的水溶液凝固点很低,可作汽车发动机的抗冻剂,故A正确;
B.丙三醇比乙二醇羟基个数多,碳原子数也多,所以丙三醇沸点应比乙二醇的沸点高,且丙三醇具有吸湿性,能用作配制化妆瓶,故B正确;
C.这两种多元醇易溶于乙醇,也易溶于水,故C错误;
D.丙三醇可以制造硝酸甘油,乙二醇是制造涤纶的主要原料,故D正确.
故选C.
点评 本题主要考查的多元醇(乙二醇和丙三醇)的性质,类比乙醇的性质以及掌握羟基的性质是关键,题目难度中等,注意硝酸甘油是炸药.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案
相关题目
16.原子结构为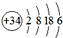 的元素,位于元素周期表的( )
的元素,位于元素周期表的( )
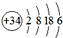 的元素,位于元素周期表的( )
的元素,位于元素周期表的( )| A. | 第六周期第Ⅳ族 | B. | 第四周期第Ⅵ族 | C. | 第六周期第ⅣA族 | D. | 第四周期第ⅥA族 |
13.某元素二价阴离子核外有10个电子,质量数为18,该元素原子的原子核中的中子数( )
| A. | 8 | B. | 10 | C. | 12 | D. | 14 |
10. 等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生氢气体
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生氢气体
积V的数据,根据数据绘制得到图,则曲线a、b、c、d所对应的实验组别可能是( )
 等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生氢气体
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生氢气体积V的数据,根据数据绘制得到图,则曲线a、b、c、d所对应的实验组别可能是( )
| 组别 | c(HCl)/(mol•L-1) | 温度/(℃) | 状态 |
| 1 | 2.0 | 30 | 块状 |
| 2 | 2.5 | 30 | 块状 |
| 3 | 2.0 | 20 | 块状 |
| 4 | 2.5 | 30 | 粉末状 |
| A. | 4、3、2、1 | B. | 4、2、1、3 | C. | 3、4、2、1 | D. | 4、1、2、3 |
17.(1)在一固定容积的密闭容器中进行着如下反应:
CO2(g)+H2(g)?CO(g)+H2O(g) 其平衡常数K和温度t的关系如下:
(a)该反应平衡常数K的表达式为:$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$;
(b)当温度为850℃,在2L密闭容器中通入1.0mol CO2和1.0mol H2,则平衡后,CO2的转化率为50%.
(2)在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-.这两步的能量变化示意图如下:
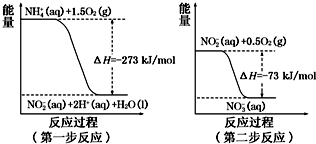
(a)第二步反应是放热反应(选填“放热”或“吸热”)
(b)1molNH4+(aq)全部氧化成NO3-(aq)的热化学方程式是NH4+ (aq)+2O2(g)═NO3- (aq)+2H+(aq)+H2O(l)△H=-346 kJ/mol.
(3)已知:
①25℃时,测得HCN和NaCN的混合溶液的pH=11,则c(HCN)/c(CN-)=2.0×10-2.
②向NaCN溶液中通入少量CO2,则发生反应的离子方程式为:CN-+CO2+H2O=HCN+HCO3-.
(4)已知:Ksp(CaCO3)=4.96×10-9,不考虑其它因素影响,现将0.40mol/L的Na2CO3溶液和0.20mol/L的CaCl2溶液等体积混合,则混合后溶液中Ca2+浓度为4.96×10-8mol/L.
CO2(g)+H2(g)?CO(g)+H2O(g) 其平衡常数K和温度t的关系如下:
| t℃ | 700 | 800 | 850 | 1000 | 1200 |
| K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
(b)当温度为850℃,在2L密闭容器中通入1.0mol CO2和1.0mol H2,则平衡后,CO2的转化率为50%.
(2)在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-.这两步的能量变化示意图如下:

(a)第二步反应是放热反应(选填“放热”或“吸热”)
(b)1molNH4+(aq)全部氧化成NO3-(aq)的热化学方程式是NH4+ (aq)+2O2(g)═NO3- (aq)+2H+(aq)+H2O(l)△H=-346 kJ/mol.
(3)已知:
| 化学式 | 电离平衡常数 |
| HCN | K=4.9×10-10 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
②向NaCN溶液中通入少量CO2,则发生反应的离子方程式为:CN-+CO2+H2O=HCN+HCO3-.
(4)已知:Ksp(CaCO3)=4.96×10-9,不考虑其它因素影响,现将0.40mol/L的Na2CO3溶液和0.20mol/L的CaCl2溶液等体积混合,则混合后溶液中Ca2+浓度为4.96×10-8mol/L.
14.向硫酸铜溶液中通入足量NH3后可得到深蓝色溶液[溶质为Cu(NH3)4SO4],再向所得溶液通入SO2至溶液呈微酸性发现有白色沉淀Q生成,反应方程式为:①2Cu(NH3)4SO4+3SO2+4H2O=2NH4CuSO3↓+3(NH4)2SO4.再将Q与足量的10mol/L硫酸混合微热,则会发生如下反应:②2NH4CuSO3+2H2SO4=Cu+(NH4)2SO4+2SO2+CuSO4+2H2O.对上述两个反应的有关分析中正确的是( )
| A. | ①是非氧化还原反应,而②是氧化还原反应 | |
| B. | 上述反应中SO2的作用只相当于催化剂 | |
| C. | 反应②中CuSO4是氧化产物 | |
| D. | 反应①中SO2发生还原反应 |
15.下列各实验中,有关浓盐酸作用的表述错误的是( )
| A. | 配制CuCl2溶液时,将CuCl2(s)溶于浓HCl后再加水冲稀,浓盐酸作用:有利于抑制CuCl2水解,可防止Cu(OH)2的形成 | |
| B. | 加热MnO2的浓HCl溶液制取氯气.浓盐酸作用:有利于减少氯气的溶解损失 | |
| C. | 浓硝酸不能溶解金,需用浓HCl溶液配制王水才能溶解金.浓盐酸作用:有利于增强Au的还原性,并且提高硝酸的氧化性 | |
| D. | 将浓硫酸滴入浓盐酸中制备HCl气体.浓盐酸作用:增大溶质的浓度,有利于促进平衡向气体溶解的逆方向移动 |
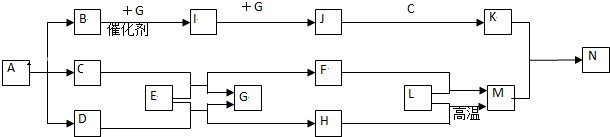
 .
. 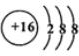 ;D与E能形成一种所有原子最外层均满足8电子的分子,该分子的结构式为S=C=S;D所在族元素的氢化物中,沸点最低的是H2S.
;D与E能形成一种所有原子最外层均满足8电子的分子,该分子的结构式为S=C=S;D所在族元素的氢化物中,沸点最低的是H2S.