题目内容
2.硫代硫酸钠俗称保险粉,又名“大苏打”.可用于照相业作定影剂、纸浆漂白作脱氯剂,也可用于氰化物、砷、汞、铅、铋、碘等中毒的治疗,也是一种常用的实验试剂.Ⅰ.已知:Na2S2O3+H2SO4=Na2SO4+S↓+SO2+H2O,某研究小组依据该反应探究外界条件对反应速率的影响,设计实验如下:
| 实验 编号 | 实验温度 /℃ | Na2S2O3 | H2SO4 | 蒸馏水体积 /mL | ||
| 体积/mL | 浓度/mol•L-1 | 体积/mL | 浓度/mol•L-1 | |||
| ① | 25 | 10 | 0.1 | 10 | 0.1 | 0 |
| ② | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
| ③ | 25 | 5 | 0.2 | 10 | 0.2 | 5 |
| ④ | 50 | 5 | 0.1 | 10 | 0.1 | 5 |
| ⑤ | 50 | 10 | 0.2 | 5 | 0.2 | 5 |
A.实验①和②探究其他条件不变时Na2S2O3浓度对相关反应速率的影响
B.实验①和③溶液变浑浊的时间相同
C.其他条件不变时,探究温度对化学反应速率的影响,应选择实验③和⑤
D.该同学在实验中采用的研究方法是实验比较法
Ⅱ.实验室用SO2通入Na2S和Na2CO3的混合溶液中来制备硫代硫酸钠.反应原理为:
2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2
本实验对Na2S纯度要求较高,利用图1所示的装置可将工业级的Na2S提纯.已知Na2S常温下微溶于酒精,加热时溶解度迅速增大,杂质不溶于酒精.提纯过程为:将已称量好的工业级Na2S放入圆底烧瓶中,加入一定质量的酒精和少量水.按图1所示装配所需仪器,向冷凝管通入冷却水,同时水浴加热.待烧瓶中固体不再减少时,停止加热.将烧瓶取下,立即趁热过滤,再冷却结晶,过滤.将所得固体洗涤、干燥,得到Na2S•9H2O晶体.
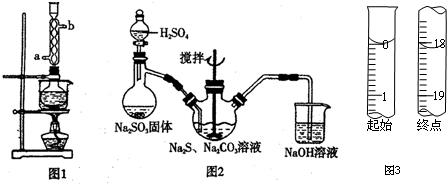
(1)在提纯过程中“趁热过滤”操作的目的是防止硫化钠结晶析出而损失、去除杂质;
(2)用图2所示装置制取Na2S2O3,其中盛放Na2SO3固体的玻璃仪器名称是蒸馏烧瓶,NaOH溶液的作用是吸收SO2等尾气,防止污染.
(3)保险粉样品中Na2S2O3•5H2O的纯度(质量分数)可通过氧化还原滴定法测定,相关反应方程式为2Na2S2O3+I2=2NaI+Na2S4O6.准确称取W g样品于锥形瓶中,用适量蒸馏水溶解,并滴加淀粉溶液作指示剂.用0.1000 mol•L?1碘的标准溶液进行滴定.
请回答:
①到达滴定终点的标志滴入最后一滴碘的标准溶液,溶液变为蓝色,且30s内不恢复原色;
②滴定起始和终点的液面位置如图3,则消耗碘的标准溶液体积为18.10mL,产品的纯度为$\frac{0.362M}{W}$%(设Na2S2O3•5H2O相对分子质量为M).
③若滴定时振荡不充分,刚看到溶液局部变色就停止滴定,则会使样品中Na2S2O3•5H2O的纯度的测量结果偏低(填“偏高”、“偏低”或“不变”).
分析 I.A.实验①、②的温度相等,c(H2SO4)相等,c(Na2S2O3)不相等,故实验①、②是探究浓度对化学反应速率的影响;
B.实验①、③的温度相等,c(Na2S2O3)相等,c(H2SO4)不相等,反应速率不相等;
C.实验③、⑤温度不相等,c(H2SO4)和c(Na2S2O3)也均不相等;
D.采取控制变量法对比实验探究外界条件对反应速率的影响;
Ⅱ.(1)过滤除去不溶杂质,若温度冷却,硫化钠会结晶析出而损失;
(2)盛放Na2SO3固体的玻璃仪器是蒸馏烧瓶,三颈烧瓶内反应结束会有未反应的二氧化硫,直接排放会污染空气;
(3)①用配制的碘溶液滴定硫代硫酸钠,利用碘单质遇碘单质变蓝指示反应终点
②终点读数与起点读数之差为消耗碘的标准溶液体积,根据方程式计算
③局部变色就停止滴定,消耗标准溶液体积偏小,测定结果偏低.
解答 解:I.A.实验①、②的温度相等,c(H2SO4)相等,c(Na2S2O3)不相等,故实验①、②是探究浓度对化学反应速率的影响,故A正确;
B.实验①、③的温度相等,c(Na2S2O3)相等,c(H2SO4)不相等,③中c(H2SO4)较大,反应速率较快,变浑浊时间较短,故B错误;
C.探究温度对化学反应速率的影响,应保证物质的浓度相等,而实验③、⑤温度不相等,c(H2SO4)和c(Na2S2O3)也均不相等,实验②、④中c(H2SO4)和c(Na2S2O3)均相等,但温度不等,故实验②、④是探究温度对化学反应速率的影响,故C错误;
D.采取控制变量法对比实验探究外界条件对反应速率的影响,故D正确,
故选:AD;
Ⅱ.(1)过滤除去不溶杂质,若温度冷却,硫化钠会结晶析出而损失,
故答案为:防止硫化钠结晶析出而损失、去除杂质;
(2)盛放Na2SO3固体的玻璃仪器是蒸馏烧瓶,三颈烧瓶内反应结束会有未反应的二氧化硫,装置中氢氧化钠是吸收尾气的主要作用,因为原料气二氧化硫是污染性气体不能排放到空气中,以防止污染空气,
故答案为:蒸馏烧瓶;吸收SO2等尾气,防止污染;
(3)①用配制的碘溶液滴定硫代硫酸钠,滴入最后一滴碘的标准溶液,溶液变为蓝色,且30s内不恢复原色,说明反应到达终点,
故答案为:滴入最后一滴碘的标准溶液,溶液变为蓝色,且30s内不恢复原色;
②终点读数为18.10mL,起点读数为0.00mL,故消耗碘的标准溶液体积为18.10mL,
设Na2S2O3•5H2O的纯度为x,则:
2Na2S2O3•5H2O~2Na2S2O3~I2
2M g 1mol
Wxg 18.10×10-3L×0.1000 mol•L-1
故2M g:Wx g=1mol:18.10×10-3L×0.1000 mol•L-1
解得x=$\frac{0.362M}{W}$%,
故答案为:18.10;$\frac{0.362M}{W}$%;
③局部变色就停止滴定,消耗标准溶液体积偏小,会使样品中Na2S2O3•5H2O的纯度的测量结果偏低,
故答案为:偏低.
点评 本题属于拼合型题目,涉及探究温度和浓度对反应速率的影响、物质实验制备、氧化还原反应滴定等,是对学生综合能力的考查,难度中等.

| A. | 60 mL 1 mol•L-1的氯化钠溶液 | B. | 30 mL 2 mol•L-1的氯化铵溶液 | ||
| C. | 60 mL 3 mol•L-1的氯化钾溶液 | D. | 30 mL 1 mol•L-1的氯化铁溶液 |
| A. | NaHSO4═Na++H++SO42- | B. | NaHCO3═Na++H++CO32- | ||
| C. | HCl═H++Cl- | D. | BaSO4═Ba2++SO42- |
| A. | 金属钠投入到水中 Na+2H2O═Na++2OH-+H2↑ | |
| B. | 碳酸氢钠溶液与盐酸反应:HCO3-+H+═CO2↑+H2 O | |
| C. | 强酸与强碱反应:H++OH-═H2O | |
| D. | CaCO3与盐酸反应:CO32-+2H+═CO2↑+H2O |
| A. | 钠和镁分别与冷水反应,判断钠和镁金属性强弱 | |
| B. | 在MgCl2与AlCl3溶液中分别加入过量的氨水,判断镁与铝的金属性强弱 | |
| C. | 硅酸钠溶液中通入CO2产生白色沉淀,判断碳酸与硅酸的酸性强弱 | |
| D. | Br2与I2分别与足量的H2反应,判断溴与碘的非金属性强弱 |
| A. | 0.2 mol•L-1 | B. | 0.4 mol•L-1 | C. | 0.25 mol•L-1 | D. | 0.5 mol•L-1 |
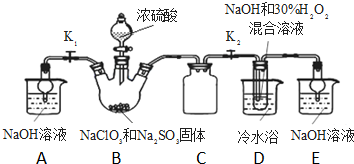 亚氯酸钠(NaClO2)是重要漂白剂.探究小组开展如下实验,回答下列问题:
亚氯酸钠(NaClO2)是重要漂白剂.探究小组开展如下实验,回答下列问题: