题目内容
4.某同学做元素周期律性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象如下表(记录现象时随手记在纸片上,不对应,需整理):| 实验方案 | 实验现象 |
| ①用砂纸擦后的镁带与沸水反应再向反应液中滴加酚酞 | A.浮于水面,熔成小球,在水面上无定向移动随之消失,溶液变成红色 |
| ②向新制的H2S饱和溶液中滴加新制的氯水 | B.产生大量气体,可在空气中燃烧,溶液变成浅红色 |
| ③钠与滴有酚酞试液的冷水反应 | C.反应不十分剧烈,产生气体可以在空气中燃烧 |
| ④镁带与2mol•L-1的盐酸反应 | D.剧烈反应,产生的气体可以在空气中燃烧 |
| ⑤铝条与2mol•L-1的盐酸反应 | E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向氯化铝溶液中滴加氢氧化钠 | F.生成淡黄色沉淀 |
(1)实验目的:验证Na、Mg、Al、S、Cl元素从左到右金属性依次减弱、非金属性依次增强的规律.
(2)实验用品:试管、酒精灯、砂纸、镊子、小刀、胶头滴管.
(3)实验内容:
| 实验方案 (填序号) | 实验现象 (填序号) | 有关化学方程式 |
(5)请用物质结构理论简单说明具有上述结论的原因同周期元素,随原子序数增大,原子核对核外电子的吸引能力逐渐增强,原子失去电子的能力逐渐减弱,得电子能力逐渐增强.
分析 (1)实验涉及Na、Mg、Al、S、Cl第三周期元素对应化合物的性质的递变规律;
(2)实验用品:试管、酒精灯、砂纸、镊子、小刀、胶头滴管;
(3)根据生成物的颜色、状态、溶液的酸碱性选取相应的实验现象;
(4)根据实验现象来分析实验的结论,涉及铜周期元素金属性、非金属性的递变规律;
(5)原子的结构决定元素的性质,利用同周期元素的原子的最外层电子数来分析.
解答 解:(1)分析每个实验可得出的结论:①③做的是镁、钠分别和水反应的实验,比较两者和水反应的难易程度,及两者碱性的强弱;②Cl2能从H2S中置换出硫;④⑤可分别得出镁、铝和盐酸置换反应的难易;⑥氢氧化铝是一种两性氢氧化物;把上述分析结果连成一个整体从中可比较出钠、镁、铝三种元素金属性强弱和氯、硫两种元素的非金属性的强弱,所以其实验目的是验证Na、Mg、Al、S、Cl元素从左到右金属性依次减弱、非金属性依次增强的规律,
故答案为:验证Na、Mg、Al、S、Cl元素从左到右金属性依次减弱、非金属性依次增强的规律;
(2)回忆每个实验过程可知,这些实验要用到的仪器有:试管、酒精灯、砂纸、镊子、小刀、胶头滴管等,故答案为:试管、酒精灯、砂纸、镊子、小刀、胶头滴管;
(3)A.浮于水面,熔成小球,四处游动,逐渐缩小,溶液变红色可知,该现象对应方案③钠与滴有酚酞试液的冷水反应,离子反应为2Na+2H2O=2Na++2OH-+H2↑,
由B.产生气体,气体可燃,溶液变浅红色可知,该现象对应的方案为①用砂纸打磨后的镁带与沸水反应,再向反应液中滴加酚酞,
由C.反应不十分强烈,产生的气体可燃可知,该现象对应的方案为⑤铝条与2mol/L的盐酸反应,
由D.剧烈反应,产生的气体可燃可知,该现象对应的方案为④镁带与2mol/L的盐酸反应,
由F.生成淡黄色沉淀可知,该现象对应的方案为②向新制的H2S饱和溶液中滴加新制的氯水,发生的离子反应为H2S+Cl2=2H++2Cl-+S↓,
由E.生成白色胶状沉淀,继而沉淀消失,该现象对应的方案为⑥向氯化铝溶液中滴加氢氧化钠,发生的反应为AlCl3+3NaOH═Al(OH)3↓+3NaCl、Al(OH)3+NaOH═NaAlO2+2H2O,
故答案为:
| 实验方案 (填序号) | 实验现象 (填序号) | 有关化学方程式 |
| ③ | A | 2Na+2H2O═2NaOH+H2↑ |
| ① | B | Mg+2H2O Mg(OH)2+H2↑ |
| ④ | D | Mg+2HCl═MgCl2+H2↑ |
| ⑤ | C | 2Al+6HCl═2AlCl3+3H2↑ |
| ⑥ | E | AlCl3+3NaOH═Al(OH)3↓+3NaCl Al(OH)3+NaOH═NaAlO2+2H2O |
| ② | F | H2S+Cl2═2HCl+S↓ |
故答案为:同周期元素随原子序数增大,元素金属性逐渐减弱,非金属性逐渐增强;
(5)同周期元素,随原子序数增大,原子核对核外最外层电子的吸引能力逐渐增强,原子失去电子的能力逐渐减弱,得电子能力逐渐增强,所以同周期元素随原子序数增大,元素金属性逐渐减弱,非金属性逐渐增强,
故答案为:同周期元素,随原子序数增大,原子核对核外电子的吸引能力逐渐增强,原子失去电子的能力逐渐减弱,得电子能力逐渐增强.
点评 本题考查学生利用实验来验证同周期元素性质的变化规律,明确现象和结论的关系及原子结构和性质的关系是解答本题的关键.

 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案| A. | 降低温度可以使平衡正向移动,可以加快反应速率 | |
| B. | 达到化学反应限度时,生成2mol NH3 | |
| C. | 向容器中再加入N2,可以加快反应速率 | |
| D. | 1mol N2 和3mol H2的总能量低于2mol NH3的总能量 |
| A. | 苯(苯酚) 加浓溴水,振荡,分液 | |
| B. | 福尔马林(甲酸) 加纯碱溶液,分液 | |
| C. | 乙醇(乙酸) 加NaOH溶液,过滤 | |
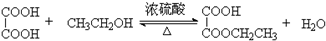
| D. | 乙酸乙酯(乙酸) 加饱和Na2CO3溶液,分液 |
| A. | 煤的干馏 | B. | 钢铁生锈 | C. | 干冰升华 | D. | 食物腐败 |
| 选项 | 实验目的 | 主要仪器 | 试剂 |
| A | 分离Br2和CCl4混合物 | 分液漏斗、烧杯 | Br2和CCl4混合物、蒸馏水 |
| B | 鉴别葡萄糖和蔗糖 | 试管、烧杯、酒精灯 | 葡萄糖溶液、蔗糖溶液、银氨溶液、水 |
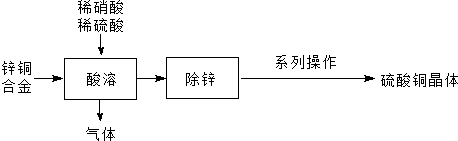
| C | 实验室制取H2 | 试管、带导管的橡皮塞 | 锌粒、稀HNO3 |
| D | 除去CH4中的C2H4 | ]试管、带导管的橡皮塞 | 酸性KMnO4溶液 |
| A. | A | B. | B | C. | C | D. | D |
 .
.
 已知A、B、C、D是中学化学中常见的四种不同微粒.它们之间存在如图中转化关系:
已知A、B、C、D是中学化学中常见的四种不同微粒.它们之间存在如图中转化关系: