题目内容
己知H2CO3的酸性强于H2S,将amol·L -1 NaHS与bmol·L-1NaOH两种稀溶液等体积混合(a>0,b>0),所得溶液中微粒间的物质的量浓度关系正确的是
| A.a=b时:c(OH-)= c(H+)+c(HS-) |
| B.a=2b时:c(S2-)>c(HS )>c(OH-)>c(H+) |
| C.a=3b时:c(Na+)+c(H+)=2c(S2-)+c(HS-)+c(OH-) |
| D.a=4b时:4c(Na+)=5c(S2-)+5c(HS-)5c(H2S) |
CD
解析试题分析:A、当两者等量混合时,溶质为Na2S,其质子守恒方程式为:c(OH-)= c(H+)+c(HS-)+2c(H2S),错误;B、当a=2b时,溶质为等物质的量的NaHS和Na2S混合,两者均水解,溶液显碱性,且以S2-的水解为主,故c(HS-)>c(S2-),错误;C、任何溶液中均存在电荷守恒,正确;D、当a=4b时,溶质为3:1的NaHS与Na2S,由物料守恒有:4n(Na)=5n(S),正确。
考点:电解质溶液、三大守恒关系

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
常温下,对下列四种溶液的叙述正确的是
| | ① | ② | ③ | ④ |
| pH | 12 | 12 | 2 | 2 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸溶液 | 盐酸 |
A.③、④两溶液相比,两者的KW相同
B.①、②两种溶液分别加水稀释100倍,pH变化较大的是①
C.等体积的③、④溶液中分别加入过量锌粒,产生的氢气前者大于后者
D.①、④ 两溶液按2: 1体积比混合后溶液中微粒浓度满足c(NH4+)+c(NH3·H2O)=c(Cl-)
常温下MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如图所示。下列叙述中不正确的是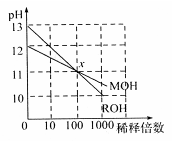
| A.ROH是一种强碱 |
| B.等物质的量浓度的MOH与盐酸反应,所得溶液呈中性,则MOH的体积大于盐酸的体积 |
| C.在x点,c(M+)=c(R+) |
| D.稀释前,c(ROH)=10 c(MOH) |
下列微粒的浓度关系一定正确的是
| A.醋酸钠和醋酸的混合溶液中:c(CH3COO-)>c (Na+)>c(H+)>c(OH一) |
| B.常温下,物质的量浓度相等的①(NH4)2SO4、②(NH4)2Fe (SO4)2、③NH4HSO4、④NH4C1溶液中c(NH4+)的大小顺序为:②>①>③>④ |
| C.pH=3的盐酸与pH=ll的氨水等体积混合液中:c(H+)=c(OH一) |
| D.某二元弱酸的酸式盐NaHA溶液中:c(H+)+c(Na+)=c(OH一)+c(HA一)+c(A2-) |
下列有关物质浓度关系的描述中,正确的是
| A.25℃时,NaB溶液的pH=8,c(Na+)-c(B-)=9.9×10-7mol·L-1 |
| B.25℃时,向0.1mol·L-1NH4HSO4溶液中滴加NaOH溶液至中性: c(Na+)>c(NH4+)>c(SO42—)>c(OH—)=c(H+) |
| C.0.1mol·L-1的NaHCO3溶液中:c(OH-)+2c(CO32-)=c(H+)+c(H2CO3) |
| D.同温下,pH相同时,溶液物质的量浓度: |
25℃时,用浓度为0.1000 mol·L-1的NaOH溶液滴定20.00 mL浓度 均为0.1000 mol·L-1的三种酸HX、HY、HZ滴定曲线如图所示。下列说法正确的是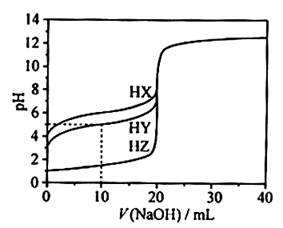
| A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ<HY<HX |
| B.根据滴定曲线,可得Ka(HY)≈10-5 |
| C.将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时: c(X-)>c(Y-)>c(OH-)>c(H+) |
D.HY与HZ混合,达到平衡时:c(H+)=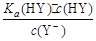 +c(Z-)+c(OH-) +c(Z-)+c(OH-) |
下列说法正确的是
| A.常温下,pH = 7的氨水与氯化铵的混合溶液中:c(Cl-) = c(NH4+) |
| B.常温下pH = 5的盐酸溶液稀释1000倍后pH = 8 |
| C.在BaSO4的饱和溶液中加入一定量Na2SO4固体,BaSO4的溶解度和Ksp均变小 |
| D.0.1 mol·L-1的硫酸铵溶液中:c(NH4+)>c(SO42-)>c(H+) |
关于10mL0.1 mol.·L-1的NH3 ? H2O溶液,下列说法正确的是
| A.25°C时,若溶液的 pH=11,则 Kb(NH3 ? H2O) = 1X10-6 mol.L-1 |
B.向溶液中加入少量CH3COONa固体,溶液中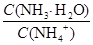 的值变小 的值变小 |
| C.向溶液中加入10mL 0.1 mol.L-1HC1,所得溶液中离子浓度大小顺序为C(NH4+)>C(Cl-)>C(H+)>C(OH-) |
| D.向溶液中加入5mL0.1mol/LHC1,所得溶液中离子的浓度一定符合:c(NH4+)+c(H+)=c(Cl-)+c(OH-) |
下列叙述正确的是
| A.0.1 mol·L-1醋酸溶液中:c(H+)= c(CH3COO-)+c(OH-) |
| B.中和pH与体积都相同的硫酸和醋酸,消耗NaOH的量后者大于前者 |
| C.同温同浓度的NaOH和澄清石灰水中,水的电离程度相同 |
| D.NaHCO3溶液中:c(Na+)>c(HCO3-)>c(H2CO3)>c(OH-)>c(H+) |