题目内容
常温下MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如图所示。下列叙述中不正确的是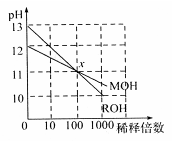
| A.ROH是一种强碱 |
| B.等物质的量浓度的MOH与盐酸反应,所得溶液呈中性,则MOH的体积大于盐酸的体积 |
| C.在x点,c(M+)=c(R+) |
| D.稀释前,c(ROH)=10 c(MOH) |
A
解析试题分析:A、结合图像ROH稀释1000倍,pH下降3,应为强碱,MOH为弱碱,正确;B、MOH的体积等于盐酸的体积时恰好完全反应,生成强酸弱碱盐,溶液呈酸性,所得溶液呈中性,则MOH的体积大于盐酸的体积,正确;C、在x点,两溶液中c(H+)、c(OH-)分别相同,结合溶液中电荷守恒,c(M+)+c(H+)=c(OH-)、c(R+)+ c(H+)=c(OH-),c(M+)=c(R+),正确;D、MOH为弱碱越稀越电离,当其浓度只有ROH的1/10时,pH>12,错误。
考点:考查强弱电解质的溶液中电离平衡,盐类水解等。

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目
图示化学变化的类型属于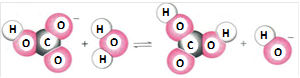
| A.取代 | B.水解 | C.中和 | D.电离 |
下列实验方案不可行或结论不正确的是
| A.用润湿的pH试纸测定饱和Na2CO3溶液pH |
B.通过观察图中导管水柱的变化,验证铁钉生锈的原因主要是吸氧腐蚀 |
| C.向Mg(OH)2悬浊液中滴加FeCl3溶液,出现红褐色沉淀,说明溶解度:Fe(OH)3<Mg(OH)2 |
| D.向同pH、同体积的醋酸和盐酸溶液中加入足量镁粉,通过完全反应后收集到的H2体积比较两种酸的电离程度:醋酸<盐酸 |
常温下,用Na2SO3溶液吸收SO2时,溶液pH随n(SO32-):n(HSO3-)变化的关系如下表:
| n(SO32-):n(HSO3-) | 91:1 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
以下离子浓度关系的判断正确的是
A.NaHSO3溶液中c(H+)<c(OH-)
B.Na2SO3溶液中c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)>c(H+)
C.当吸收液呈中性时,c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)=c(H+)
D.当吸收液呈中性时,c(Na+)= c(HSO3-)+2 c(SO32-)
某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是( )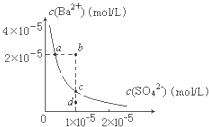
| A.加入Na2SO4可使溶液由a点变到b点 |
| B.通过蒸发可以使溶液由d点变到c点 |
| C.d点无BaSO4沉淀生成 |
| D.a点对应的Ksp大于c点对应的Ksp |
下列有关溶液的说法正确的是
| A.向10mLpH=3的酣酸溶液中加入10mLpH=l1的NaOH溶液,混合液的pH=7 |
| B.实验测定NH4HCO3溶液显碱性,CH3COONH4溶液显中性,说明酸性CH3COOH>HCO3 |
| C.NH4CI溶液加水稀释过程中c(H+)+c(NH3·H2O)=c(OH一) |
| D.向AgI沉淀中加人饱和KCl溶液,有白色沉淀生成,说明AgCl比AgI更难溶 |
关于电解质溶液下列说法中不正确的是
A.向浓度均为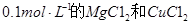 混合溶液中逐滴加入氨水,先生成蓝色 混合溶液中逐滴加入氨水,先生成蓝色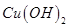 沉淀,则 沉淀,则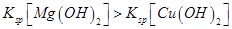 |
| B.用等浓度的NaOH溶液中和等体积pH=2与pH=3的醋酸,所消耗的NaOH溶液的体积前者是后者的10倍 |
C.由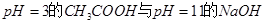 溶液等体积混合,其离子浓度的顺序为: 溶液等体积混合,其离子浓度的顺序为: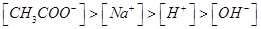 |
D.某温度下纯水中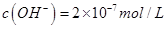 ,则该温度下0.1mol/L的盐酸的pH=1 ,则该温度下0.1mol/L的盐酸的pH=1 |
己知H2CO3的酸性强于H2S,将amol·L -1 NaHS与bmol·L-1NaOH两种稀溶液等体积混合(a>0,b>0),所得溶液中微粒间的物质的量浓度关系正确的是
| A.a=b时:c(OH-)= c(H+)+c(HS-) |
| B.a=2b时:c(S2-)>c(HS )>c(OH-)>c(H+) |
| C.a=3b时:c(Na+)+c(H+)=2c(S2-)+c(HS-)+c(OH-) |
| D.a=4b时:4c(Na+)=5c(S2-)+5c(HS-)5c(H2S) |
常温下,有关醋酸溶液的叙述中错误的是
| A.pH=5.6的CH3COOH与CH3COONa混合溶液中:c(Na+)<c(CH3COOˉ) |
| B.将pH=3的醋酸稀释为pH=4的过程中,c(CH3COOH)/ c(H+)比值不变 |
| C.浓度均为0.1mol/L的CH3COOH与CH3COONa溶液等体积混合后:c(CH3COOˉ)+ c(CH3COOH)="2" c(Na+) |
| D.amLpH=3的醋酸溶液与bmLpH=11的NaOH溶液恰好完全中和时,a=b |