题目内容
4.设NA为阿伏加德罗常数的值.下列说法正确的是( )| A. | 0.1 mol•L-1的Na2S溶液中,S2-的数目小于0.1 NA | |
| B. | 0.1 mol丙烷中含有的共价键数目为0.8 NA | |
| C. | 标准状况下,11.2 L甲醇中含有的分子数目为0.5 NA | |
| D. | 0.1 mol氧化钠和过氧化钠的混合物中含有的离子总数为0.3 NA |
分析 A、溶液体积不明确;
B、1mol丙烷中含10mol共价键;
C、标况下,甲醇为液态;
D、Na2O和Na2O2均由2个阳离子和1个阴离子构成.
解答 解:A、溶液体积不明确,故S2-的个数无法计算,故A错误;
B、1mol丙烷中含10mol共价键,故0.1mol丙烷中含1mol共价键,即NA个,故B错误;
C、标况下,甲醇为液态,故甲醇的物质的量无法计算,故C错误;
D、Na2O和Na2O2均由2个阳离子和1个阴离子构成,故0.1molNa2O和Na2O2的混合物中,无论两者的比例如何,其含有的离子均为0.3mol,个数为0.3NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.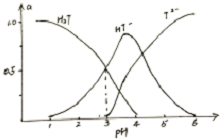 酒石酸是葡萄酒中特有的一种有机酸,葡萄酒的pH主要取决于酒石酸的含量,正常的葡萄酒pH约为2.9-3.8.常温下,酒石酸(用H2T表示)水溶液中三种微粒所占分数(a)与pH关系如图所示.下列表述不正确是( )
酒石酸是葡萄酒中特有的一种有机酸,葡萄酒的pH主要取决于酒石酸的含量,正常的葡萄酒pH约为2.9-3.8.常温下,酒石酸(用H2T表示)水溶液中三种微粒所占分数(a)与pH关系如图所示.下列表述不正确是( )
 酒石酸是葡萄酒中特有的一种有机酸,葡萄酒的pH主要取决于酒石酸的含量,正常的葡萄酒pH约为2.9-3.8.常温下,酒石酸(用H2T表示)水溶液中三种微粒所占分数(a)与pH关系如图所示.下列表述不正确是( )
酒石酸是葡萄酒中特有的一种有机酸,葡萄酒的pH主要取决于酒石酸的含量,正常的葡萄酒pH约为2.9-3.8.常温下,酒石酸(用H2T表示)水溶液中三种微粒所占分数(a)与pH关系如图所示.下列表述不正确是( )| A. | 常温下,H2T?H++HT- Ka=10-3 | |
| B. | 当HT-和T2-物质的量浓度相等时,溶液中水电离出的H+浓度大于纯水中H+的浓度 | |
| C. | 当葡萄酒的pH为3.7时,HT-所占分数达到最大,此时葡萄酒中c(H2T)<c(T2-) | |
| D. | 葡萄酒中除了存在酒石酸外,还存在酒石酸盐 |
15.下列物质溶于水因水解而使溶液呈酸性的是( )
| A. | SO2 | B. | NaHSO3 | C. | CH3COONa | D. | FeCl2 |
19.下列说法正确的是( )
| A. | 按系统命名法,有机物 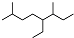 可命名为3,7-二甲基-4-乙基辛烷 可命名为3,7-二甲基-4-乙基辛烷 | |
| B. | 环己醇分子中所有的原子可能共平面 | |
| C. | 谷氨酸分子(α-氨基戊二酸)缩合只能形成1种二肽(不考虑立体异构) | |
| D. | 在一定条件下,1.0 mol的  最多能与含3.0 mol NaOH的溶液完全反应 最多能与含3.0 mol NaOH的溶液完全反应 |
4.图为两种途径制备硫酸的过程,反应条件略.下列说法不正确的是( )


| A. | 含l mol H2SO4的浓溶液与足量NaOH反应,放出的热量即为中和热 | |
| B. | 途径②增大O2浓度可提高SO2转化率 | |
| C. | 途径②中SO2和SO3均属于酸性氧化物 | |
| D. | 若△Hl<△H2+△H3,则2H2O2(aq)=2H2O(1)+O2 (g)为放热反应 |
2.下列对三种有机物的叙述不正确的是( )
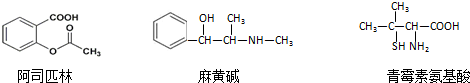

| A. | 三种有机物都能发生酯化反应 | |
| B. | 阿司匹林的苯环上的一氯代物有8种 | |
| C. | 麻黄碱的分子式是C10H15NO,苯环上的一硝基取代物有3种 | |
| D. | 青霉素氨基酸既能与盐酸反应,又能与NaOH溶液反应 |
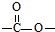 ”结构存在的同分异构体的数目有( )
”结构存在的同分异构体的数目有( )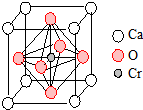 翡翠的主要成分为NaAlSi2O6,还含有其他多种金属阳离子,其中Cr3+的含量决定其绿色的深浅.
翡翠的主要成分为NaAlSi2O6,还含有其他多种金属阳离子,其中Cr3+的含量决定其绿色的深浅.
 +2H2O.
+2H2O.