��Ŀ����
8����ѧ��ҵ���������������ϢϢ��أ��ش��������⣺��1����֪��Ӧ��Fe��s��+CO2��g��?FeO��s��+CO��g����H=a kJ?mol-1��ƽ�ⳣ��ΪK��
����ڲ�ͬ�¶��£�Kֵ���£�
| �¶�/�� | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
�ڷ�Ӧ�е�a����0������ڡ�����С�ڡ����ڡ�����
����500��ʱ���з�Ӧ��CO2��ʼŨ��Ϊ2mol?L-1��CO��ƽ��Ũ��Ϊ1mol?L-1��
��700�淴Ӧ�ﵽƽ�⣬��ʱ����Ӧ��CO��Ũ�ȣ���ƽ���ƶ���ﵽ�µ�ƽ�⣬������������ʱ��CO ��CO2�������ֵ���䣨���������С�����䡱����
��2����ҵ�̵���Ӧ�ǣ�N2��g��+3H2��g��?2NH3��g����H=-92.4kJ/mol������ͬ�¶��£������Ϊ0.25L�����������ܱ������пɷ����������淴Ӧ����÷�Ӧ���й����������
| ���� ��� | ��ʼʱ���������ʵ���/mol | ��ƽ��ʱ��ϵ�� �����仯 | ||
| N2 | H2 | NH3 | ||
| a | 1 | 3 | 0 | ����23.1kJ |
| b | 0.6 | 1.8 | 0.8 | ����Q kJ |
������b��ƽ��ʱNH3��ƽ��Ũ��c��NH3��=2mol?L-1��
������������ȷ����AB��
A������a��ƽ��ʱNH3�����ʵ�����0.5mol
B������b��ʼ����ϳɰ����淴Ӧ�������
C��������a�����Ϊ0.2L�����ƽ��ʱ�ų�������С��23.1kJ
D������������֪���ݼ�������b��ƽ�ⳣ����
���� ��1����ƽ�ⳣ������������Ũ��ϵ������֮�����Է�Ӧ��Ũ��ϵ������֮����
���ɱ������ݿ�֪�������¶ȣ�ƽ�ⳣ������Ӧ������Ӧ�����ƶ����ݴ��жϣ�
���ɱ������ݿ�֪�������¶ȣ�ƽ�ⳣ������Ӧ������Ӧ�����ƶ����ݴ��жϣ�
�ܸ���ƽ�ⳣ��ֻ���¶�Ӱ�죬���¶Ȳ���ʱ��ƽ�ⳣ�����䣬���ݷ�Ӧ����ʽ��֪���÷�Ӧ��ƽ�ⳣ������CO ��CO2������ȣ��ݴ˴��⣻
��2���ӵ�Чƽ��ĽǶȷ�����0.6molN2��1.8molH2��0.8molNH3�൱1molN2��3molH2������ͬ�����´�����ͬƽ��״̬������ƽ��ʱ����������N2��ƽ��Ũ��c��N2����NH3��ƽ��Ũ��c��NH3����ȣ��ݴ˷������㣻
��� �⣺��1����ƽ�ⳣ������������Ũ��ϵ������֮�����Է�Ӧ��Ũ��ϵ������֮��������K=$\frac{[CO]}{[CO2]}$��
�ʴ�Ϊ��$\frac{[CO]}{[CO2]}$��
���ɱ������ݿ�֪�������¶ȣ�ƽ�ⳣ������Ӧ������Ӧ�����ƶ���������ӦΪ���ȷ�Ӧ����a��0��
�ʴ�Ϊ�����ڣ�
����ƽ��ʱCO��Ũ��Ϊamol/L���ɷ���ʽ��֪��������̼��Ũ�ȱ仯��Ϊamol/L����ƽ��ʱ������̼��Ũ��Ϊ��2-a��mol/L��500��ʱƽ�ⳣ��Ϊ1����$\frac{a}{2-a}$=1�����a=1��
�ʴ�Ϊ��1��
�ܸ���ƽ�ⳣ��ֻ���¶�Ӱ�죬���¶Ȳ���ʱ��ƽ�ⳣ�����䣬���ݷ�Ӧ����ʽ��֪���÷�Ӧ��ƽ�ⳣ������CO ��CO2������ȣ���������Ӧ��CO��Ũ�ȣ���ƽ���ƶ���ﵽ�µ�ƽ�⣬CO ��CO2������Ȳ��䣬
�ʴ�Ϊ�����䣻
��2���ӵ�Чƽ��ĽǶȷ�����0.6molN2��1.8molH2��0.8molNH3�൱1molN2��3molH2������ͬ�����´�����ͬƽ��״̬������ƽ��ʱ����������N2��ƽ��Ũ��c��N2����NH3��ƽ��Ũ��c��NH3����ȣ�
�� N2��g��+3H2��g��?2NH3��g����H=-92.4kJ/mol
��ʼ��1 3 0 92.4kJ
�仯��0.25 0.75 0.5 23.1kJ
ƽ�⣺0.75 2.25 0.5
����������a��ƽ��ʱN2��ƽ��Ũ��c��N2��=$\frac{0.75mol}{0.25L}$=3mol/L��
�ʴ�Ϊ��3��
����������b��ƽ��ʱNH3��ƽ��Ũ��c��NH3��=$\frac{0.5mol}{0.25L}$=2mol/L��
�ʴ�Ϊ��2��
��A���������Ϸ���������a��ƽ��ʱNH3�����ʵ�����0.5mol������ȷ��
B���������Ϸ�����ƽ��ʱNH3�����ʵ�����0.5mol����������b��ʼ����ϳɰ����淴Ӧ������У�����ȷ��
C��������a�����Ϊ0.2L������С�����ƽ��������Ӧ�����ƶ������ƽ��ʱ�ų�����������23.1kJ���ʴ���
D����Ϊa��b����ͬ�����´�����ͬƽ��״̬��������������֪���ݼ�������b��ƽ�ⳣ�����ʴ���
��ѡ��AB��
���� ���⿼���˻�ѧƽ��Ӱ�����ء�ƽ�ⳣ����Ӧ�á��ϳɰ���Ӧ������ѡ��Ӱ�컯ѧƽ������أ���Ŀ�Ѷ��еȣ������ڻ���֪ʶ���ۺ�Ӧ�ÿ��飬ע�����K���¶ȵĹ�ϵ�Լ�Ӱ�컯ѧƽ������أ�

 Ӯ�ڿ�����ʦ��ʱ�ƻ�ϵ�д�
Ӯ�ڿ�����ʦ��ʱ�ƻ�ϵ�д� �������Ͽ�ʱͬ��ѵ��ϵ�д�
�������Ͽ�ʱͬ��ѵ��ϵ�д�| A�� | ����A��B��ת����֮��һ����1��2 | |
| B�� | ��ʼʱ�̺ʹ�ƽ��������е�ѹǿ��Ϊ1��1 | |
| C�� | ����ʼ����3molA��3molB�����ƽ��ʱ����3amolC | |
| D�� | ��v����A��=v����C��ʱ���ɶ϶���Ӧ�ﵽƽ�� |
| A�� | ���������ݻ����䣬�����м���1molH2��ƽ�ⳣ����С | |
| B�� | ���������ݻ����䣬�����м���1molHe�����淴Ӧ���ʾ����� | |
| C�� | ��������������ѹǿ���䣬�����м���1molHe����Ӧ���ʾ���С | |
| D�� | ��������������ѹǿ���䣬�������м���1molH2��1mol��2�����´�ƽ�⣬H2�����������С |
| �������� | �����Լ� | ʵ������ | ���ӷ���ʽ |
| ��CO32- | �����ݲ��� | ||
| ��SO42- | ������ɫ���� | ||
| ��Cl- | ������ɫ���� |

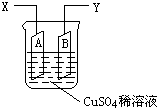 ��ͼ�ǿ����ڲ��������ӵ�������װ��ʾ��ͼ������A�Ǵ�ͭƬ��B��ʯī������100mLCuSO4ϡ��Һ�У�ͭƬ��ʯī���������������������˷ֱ�ΪX��Y��
��ͼ�ǿ����ڲ��������ӵ�������װ��ʾ��ͼ������A�Ǵ�ͭƬ��B��ʯī������100mLCuSO4ϡ��Һ�У�ͭƬ��ʯī���������������������˷ֱ�ΪX��Y��