题目内容
20.某溶液有Cl-、CO32-、SO42-,要求依次检验出这三种离子,请完成下列设计:| 检验离子 | 所加试剂 | 实验现象 | 离子方程式 |
| ①CO32- | 有气泡产生 | ||
| ②SO42- | 产生白色沉淀 | ||
| ③Cl- | 产生白色沉淀 |
分析 用三种试剂将三种离子检验出来,每加一种试剂能够检验出一种离子,此时要注意每加入一种试剂只能与一种离子结合,检验氯离子可以使用银离子,检验硫酸根离子可以使用钡离子,检验碳酸根离子可以使用氢离子,而银离子和钡离子都可以与碳酸根离子结合成沉淀,所以需先检验碳酸根离子,此时可以加入稀硝酸,检验氯离子所用的银离子可以与硫酸根离子结合成微溶于水的硫酸银,所以需先检验钡离子,此时可以加入硝酸钡,最后检验银离子,可以加入硝酸银.
解答 解:依次检验出这三种离子,应排除离子之间的干扰,先加足量硝酸液,生成气泡,确定CO32-存在,反应的离子方程式为CO32-+2H+═CO2↑+H2O;再加足量硝酸钡溶液,观察到白色沉淀,则确定SO42-存在,反应的离子方程式为:Ba2++SO42-═BaSO4↓;过滤后向滤液中加 硝酸银溶液,现象是生成白色沉淀,确定Cl-存在,反应的离子方程式为:Ag++Cl-═AlgCl↓,
故答案为:
| 检验离子 | 所加试剂 | 离子方程式 | |
| ①CO32- | 稀硝酸 | CO32-+2H+═CO2↑+H2O | |
| ②SO42- | 硝酸钡溶液 | Ba2++SO42-═BaSO4↓ | |
| ③Cl- | 硝酸银溶液 | Ag++Cl-═AlgCl↓ |
点评 本题考查常见离子的检验方法,题目难度中等,明确氧化还原反应中元素的化合价变化、常见离子的检验方法即可解答,注意检验离子应排除干扰及先后检验出离子.

练习册系列答案
相关题目
6.下列物质中存在的化学键,在熔化时没有破坏的是( )
| A. | 金属铜 | B. | 碘 | C. | 固体氮 | D. | 硫酸钠 |
11.阱(N 2H4)常用于火箭或原电池的燃料.己知:
①N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol
②N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-534.0kJ•mol
③H2O(g)=H2O(1)△H=-44kJ/mol
(1)2N2H4(g)+2NO2(g)=3N2(g)+4H2O(1)△H=-1311.7kJ.mol-1
(2)一定温度下,将N2H4与N02以体积比1:1置于10L密闭容器中发生反应:2N2H4(g)+2NO2(g)=3N2(g)+4H2O(1)
下列不能说明反应达到平衡状态的是ac.(填序号)
a.混合气体密度保持不变 b.混合气体颜色保持不变
c.N2H4比与NO2体积比保持不变 d.体系压强保持不变
(3)在10L的密闭容器中发生上述反应,容器内部分物质的物质的量变化如下表:
前2min内NO2的平均反应速率为0.01mol/(L•min).平衡时N02的转化率25%;(2)中反应平衡常数表达式为K=$\frac{{c}^{3}({N}_{2})}{{c}^{2}({N}_{2}{H}_{4})•{c}^{2}(N{O}_{2})}$,计算该温度下反应的平衡常数K=0.9375.反应在第6min时改变了条件,改变的条件可能是bc(填序号)a.使用催化剂b.升高温度c.扩大容器容积d.增加N02的量
(4)若在一定温度下,(2)中反应的平衡常数为20,反应到某时刻测得N2H4、NO2、N2的溶度均为0.1mol.L-1,此时v正>v逆.
①N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol
②N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-534.0kJ•mol
③H2O(g)=H2O(1)△H=-44kJ/mol
(1)2N2H4(g)+2NO2(g)=3N2(g)+4H2O(1)△H=-1311.7kJ.mol-1
(2)一定温度下,将N2H4与N02以体积比1:1置于10L密闭容器中发生反应:2N2H4(g)+2NO2(g)=3N2(g)+4H2O(1)
下列不能说明反应达到平衡状态的是ac.(填序号)
a.混合气体密度保持不变 b.混合气体颜色保持不变
c.N2H4比与NO2体积比保持不变 d.体系压强保持不变
(3)在10L的密闭容器中发生上述反应,容器内部分物质的物质的量变化如下表:
| 物质的量/时间 | n(N2H4) | n(NO2) | n(N2) |
| 起始 | 0.8 | 1.6 | 0 |
| 第2min | 0.6 | a | 0.3 |
| 第5min | 0.4 | 1.2 | 0.6 |
| 第6min | 0.4 | 1.2 | 0.6 |
| 第10min | 0.6 | 1.4 | 0.3 |
(4)若在一定温度下,(2)中反应的平衡常数为20,反应到某时刻测得N2H4、NO2、N2的溶度均为0.1mol.L-1,此时v正>v逆.
8.化学工业与人类的生产生活息息相关,回答下列问题:
(1)已知反应:Fe(s)+CO2(g)?FeO(s)+CO(g)△H=a kJ?mol-1,平衡常数为K;
测得在不同温度下,K值如下:
①写出K的表达式$\frac{[CO]}{[CO2]}$.
②反应中的a大于0(填“大于”、“小于”或“等于”).
③若500℃时进行反应,CO2起始浓度为2mol?L-1,CO的平衡浓度为1mol?L-1.
④700℃反应达到平衡,此时增大反应中CO的浓度,该平衡移动后达到新的平衡,其它条件不变时,CO 和CO2的体积比值不变(填“增大”、“减小”或“不变”).
(2)工业固氮反应是:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol.在相同温度下,体积均为0.25L的两个恒容密闭容器中可发生上述可逆反应,测得反应的有关数据如表:
①容器a达平衡时N2的平衡浓度c(N2)=3mol?L-1.
②容器b达平衡时NH3的平衡浓度c(NH3)=2mol?L-1.
③下列叙述正确的是AB.
A.容器a达平衡时NH3的物质的量是0.5mol
B.容器b开始是向合成氨的逆反应方向进行
C.若容器a体积变为0.2L,则达平衡时放出的热量小于23.1kJ
D.不能利用已知数据计算容器b的平衡常数.
(1)已知反应:Fe(s)+CO2(g)?FeO(s)+CO(g)△H=a kJ?mol-1,平衡常数为K;
测得在不同温度下,K值如下:
| 温度/℃ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
②反应中的a大于0(填“大于”、“小于”或“等于”).
③若500℃时进行反应,CO2起始浓度为2mol?L-1,CO的平衡浓度为1mol?L-1.
④700℃反应达到平衡,此时增大反应中CO的浓度,该平衡移动后达到新的平衡,其它条件不变时,CO 和CO2的体积比值不变(填“增大”、“减小”或“不变”).
(2)工业固氮反应是:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol.在相同温度下,体积均为0.25L的两个恒容密闭容器中可发生上述可逆反应,测得反应的有关数据如表:
| 容器 编号 | 起始时各物质物质的量/mol | 达平衡时体系的 能量变化 | ||
| N2 | H2 | NH3 | ||
| a | 1 | 3 | 0 | 放热23.1kJ |
| b | 0.6 | 1.8 | 0.8 | 吸热Q kJ |
②容器b达平衡时NH3的平衡浓度c(NH3)=2mol?L-1.
③下列叙述正确的是AB.
A.容器a达平衡时NH3的物质的量是0.5mol
B.容器b开始是向合成氨的逆反应方向进行
C.若容器a体积变为0.2L,则达平衡时放出的热量小于23.1kJ
D.不能利用已知数据计算容器b的平衡常数.
5.下列说法正确的是( )
| A. | 原子晶体中只存在非极性共价键 | |
| B. | 干冰升华时,分子内共价键不会发生断裂 | |
| C. | 因为HCl的相对分子质量大于HF,所以HCl的沸点高于HF | |
| D. | 金属元素和非金属元素形成的化合物一定是离子化合物 |
12.在一定温度下,向不同电解质溶液中加入新物质时,其电流强度(I)随新物质加入量(m)的变化曲线不正确的是( )
| A. | 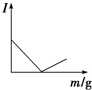 向Ba(OH)2溶液中逐滴加入等浓度的H2SO4至过量 | |
| B. | 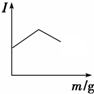 向醋酸溶液中逐滴加入等浓度的氨水至过量 | |
| C. | 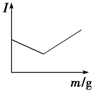 向盐酸溶液中逐滴加入等浓度的NaOH溶液至过量 | |
| D. | 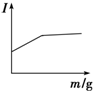 向氨水中逐滴加入等浓度的盐酸至过量 |
10.根据以下叙述制备氯化铜:先将浓盐酸用蒸气加热至80℃左右,慢慢加入含有FeO、Fe2O3杂质的CuO粉,充分反应,使其溶解.已知:
为了除去溶液中的铁元素,可采用的试剂是( )
| 溶液中被沉淀离子 | Fe3+ | Fe2+ | Cu2+ |
| 完全生成氢氧化物沉淀时,溶液的pH | ≥3.7 | ≥9.6 | ≥6.4 |
| A. | NaOH溶液 | B. | 氨水 | C. | H2O2、Cu2(OH)2CO3 | D. | KMnO4、CuO |