��Ŀ����
����Ŀ��(1)���������������������֣�
��________�������Բ����������ϣ�
��________�������Ա���¶��ѷŲ��������⣻
��_____��������ʹ���������С���ܳ�������ԭ���Լ������������ŵ㡣
(2)��������������Դ���ִ�����ɺ��ӵ���Ҫ�����ٳ����������������õ�һ��������_________��
(3)������������������Ҫ���������з��࣬һȺ����־Ը����ij�����ƹ��������࣬������������������һЩ�з����־�����������䣬���ȴ�������������û�з�����á�������������ԭ�������________��
A.�������鷳��û�����������ϰ�� B.����ÿ��������������dz���
C.����Ļ�����ʶ��ǿ D.���������������ı�
(4)
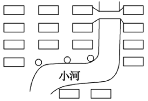
��ͼ��ij����С���������ռ���(СԲȦ)�IJ��֣�����ѡַ�ϴ��ڵ�����������_________��________�������ռ���ѡַӦ���ǵ����ذ���(�������)________��________��________��
���𰸡��ѷ� �������� ���� ��������ȡȼ����(���ֽ�����������츴�ϰ壻�ϲ���ƿ���첣��˿�ȣ����������𰸾���) ACD �����ռ���ֲ������� �����ռ����غ����ã���ȾˮԴ(���������𰸾���) �Ƿ���ھ���Ͷ������ �Ƿ�Ӱ���������� �Ƿ�Ӱ��������ľ���[�Ƿ�����ٴ���
Ⱦ���Ƿ�����������������(��ѡ3�㣬���������𰸾���)]
��������
�������ϲ������漰ǧ������Ҫ���ϴ����������ķ���������������á����������ա�Ϊ�˻���������������������������ռ������䡢�����ۺϿ��ǣ����ڴﵽ�������á�����������Ŀ�ġ�
(1)���������������������֣�
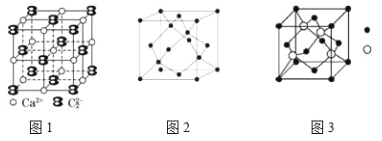
�ٱ������������������ȣ����Բ����������ϣ���������Ϊ�ѷʷ�����Ϊ���ѷʣ�
�ڱ��罨������������ռ�ض࣬Ӧ����¶��ѷţ���������Ϊ����������Ϊ����������
����������к��н϶����Ҷ����֦����ݣ���ʹ���������С������������ԭ���Լ����ò����������ȣ���������Ϊ���շ�����Ϊ�����գ�
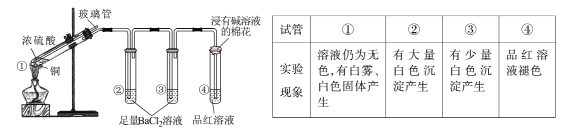
(2)���������������õ�����Ϊ����������ȡȼ����(���ֽ�����������츴�ϰ壻�ϲ���ƿ���첣��˿�ȣ����������𰸾���)����Ϊ����������ȡȼ����(���ֽ�����������츴�ϰ壻�ϲ���ƿ���첣��˿�ȣ����������𰸾���)��
(3)�������û�н�����������ã�������������ԭ������Ǿ������鷳��û�����������ϰ�ߡ�����ÿ��������������dz��ࡢ���������������ı��ȡ���Ϊ��ACD��
(4)ͼ�������ռ�����ּ��У�����Щ����Һ�Զ���ҿ���ˮԴ������ѡַ�ϴ��ڵ����������������ռ���ֲ������Ⱥ������ռ����غ����ã���ȾˮԴ(���������𰸾���)�������ռ���ѡַӦ���ǵ����ذ���(�������)���Ƿ���ھ���Ͷ���������Ƿ�Ӱ����������Ƿ�Ӱ��������ľ���[�Ƿ�����ٴ���Ⱦ���Ƿ�����������������(��ѡ3�㣬���������𰸾���)]����Ϊ�������ռ���ֲ������ȣ������ռ����غ����ã���ȾˮԴ(���������𰸾���)���Ƿ���ھ���Ͷ���������Ƿ�Ӱ����������Ƿ�Ӱ��������ľ���[�Ƿ�����ٴ���Ⱦ���Ƿ�����������������(��ѡ3�㣬���������𰸾���)]��

 Ӣ�żƻ���ĩ����ϵ�д�
Ӣ�żƻ���ĩ����ϵ�д� ��Ӣ���㿨ϵ�д�
��Ӣ���㿨ϵ�д�