题目内容
9.铝硅合金材料性能优良.铝土矿(含30% SiO2、40.8% Al2O3和少量Fe2O3等)干法制取该合金的工艺如图1: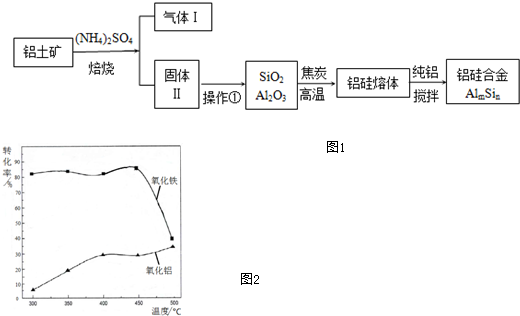
(1)若湿法处理铝土矿,用强酸浸取时,所得溶液中阳离子有Al3+、Fe3+、H+.
(2)铝硅合金材料中若含铁,会影响其抗腐蚀性.原因是铁与铝形成原电池,加快了铝的腐蚀.
(3)焙烧除铁反应:4(NH4)2SO4+Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$2NH4Fe(SO4)2+3H2O+6NH3↑(Al2O3部分发生类似反应).氧化物转化为硫酸盐的百分率与温度的关系如图2,最适宜焙烧温度为300℃.指出气体Ⅰ的用途制氮肥、用硫酸吸收气体(氨气)循环到焙烧过程中等(任写一种).
(4)操作①包括:加水溶解、过滤.若所得溶液中加入过量NaOH溶液,含铝微粒发生反应的离子方程式为Al3++4OH-=AlO2-+2H2O.
(5)用焦炭还原SiO2、Al2O3会产生中间体SiC、Al4C3.任写一个高温下中间体又与Al2O3反应生成铝、硅单质的化学方程式Al4C3+Al2O3$\frac{\underline{\;高温\;}}{\;}$6Al+3CO↑.
(6)不计损失,投入1t铝土矿,当加入27kg纯铝后,铝硅合金中m:n=9:5.(摩尔质量:SiO2---60g/mol Al2O3---102g/mol)
分析 铝土矿(含30% SiO2、40.8% Al2O3和少量Fe2O3等)加硫酸铵焙烧,Fe2O3转化为NH4Fe(SO4)2同时生成氨气,加水溶解、过滤,滤渣为SiO2和Al2O3,用焦炭在高温条件下还原SiO2、Al2O3得到硅铝熔体,在加纯铝搅拌,得到硅铝合金;
(1)铝土矿中的氧化铝和氧化铁能溶于强酸;
(2)Al、Fe形成原电池,活泼性强的做负极;
(3)焙烧时尽可能是氧化铁反应,而氧化铝不反应;氨气可以制氮肥,也可以制备硫酸铵循环利用;
(4)根据流程分析解答;溶液中含有铝离子与氢氧根离子生成偏铝酸根离子;
(5)在高温条件下,Al4C3与Al2O3反应生成Al和CO;
(6)铝土矿中含30% SiO2、40.8% Al2O3,又加入27kg纯铝,根据质量守恒计算铝硅的质量和质量比.
解答 解:铝土矿(含30% SiO2、40.8% Al2O3和少量Fe2O3等)加硫酸铵焙烧,Fe2O3转化为NH4Fe(SO4)2同时生成氨气,加水溶解、过滤,滤渣为SiO2和Al2O3,用焦炭在高温条件下还原SiO2、Al2O3得到硅铝熔体,在加纯铝搅拌,得到硅铝合金;
(1)铝土矿中的氧化铝和氧化铁能溶于强酸生成Al3+、Fe3+,另外还有剩余的H+,所以溶液中的阳离子有Al3+、Fe3+、H+;
故答案为:Al3+、Fe3+、H+;
(2)Al、Fe形成原电池,Al活泼性比Fe强的做负极,被腐蚀,所以铝硅合金材料中若含铁,容易发生电化学腐蚀;
故答案为:铁与铝形成原电池,加快了铝的腐蚀;
(3)焙烧时尽可能是氧化铁反应,而氧化铝不反应,由图可知在300℃时,氧化铁转化为硫酸盐的百分率很高,而氧化铝转化为硫酸盐的百分率最低,所以最适宜焙烧温度为300℃;气体Ⅰ为氨气,氨气可以用于制氮肥,也可以用硫酸吸收来备硫酸铵循环到焙烧过程中;
故答案为:300℃;制氮肥、用硫酸吸收气体(氨气)循环到焙烧过程中;
(4)由流程分析可知,操作①包括:加水溶解、过滤;溶液中含有铝离子与氢氧根离子生成偏铝酸根离子,其反应的离子方程式为:Al3++4OH-=AlO2-+2H2O;
故答案为:过滤;Al3++4OH-=AlO2-+2H2O;
(5)在高温条件下,Al4C3与Al2O3反应生成Al和CO,其反应的方程式为:Al4C3+Al2O3$\frac{\underline{\;高温\;}}{\;}$6Al+3CO↑;
故答案为:Al4C3+Al2O3$\frac{\underline{\;高温\;}}{\;}$6Al+3CO↑;
(6)投入1t铝土矿,加入27kg纯铝,已知铝土矿中含30% SiO2、40.8% Al2O3,则Al的总质量为:1000kg×40.8%×$\frac{54}{102}$+27kg=243kg,
Si的总质量为1000kg×30%×$\frac{28}{60}$=140kg,则铝硅合金中m:n=$\frac{243}{27}$:$\frac{140}{28}$=9:5,
故答案为:9:5.
点评 本题考查了物质分离和提纯基本操作,注意把握流程中发生的化学反应为解答的关键,注重信息与所学知识的结合分析解决问题,侧重知识迁移应用能力的考查,题目难度中等.

 同步练习强化拓展系列答案
同步练习强化拓展系列答案| A. | H2O2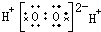 | B. | CCl4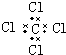 | C. | MgCl2 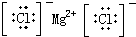 | D. | NaOH  |
| A. | 食盐和氯化氢溶于水 | B. | 钠和硫熔化 | ||
| C. | 碘和干冰升华 | D. | 二氧化硅和氧化钠熔化 |
| A. | 硒化氢不稳定 | |
| B. | 硒化氢的水溶液显弱酸性 | |
| C. | 得电子能力强于硫 | |
| D. | 其最高价氧化物的水化物酸性强于砷弱于溴 |
(1)第一份加入足量的NaOH溶液,无沉淀;加热,收集到标准状况下的气体336mL.
(2)第二份加入足量的用盐酸酸化的BaCl2溶液,产生2.33g白色沉淀,同时收集到标准状况下的气体336mL,该气体能使品红溶液褪色.
根据上述实验,下列推断正确的是( )
| A. | K+一定存在 | |
| B. | Ag+和Cl-一定不存在 | |
| C. | HCO3-一定不存在 | |
| D. | 混合溶液中一定有0.015 mol SO32- |
| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
(2)在空气中直接加热CuCl2•2H2O晶体得不到纯的无水CuCl2,而是生成Cu(OH)Cl,写出相关的化学反应方程式:CuCl2•2H2O$\frac{\underline{\;\;△\;\;}}{\;}$Cu(OH)Cl+HCl↑+H2O.由CuCl2•2H2O晶体得到纯的无水CuCl2的合理方法是在干燥HCl气流中加热制得.
(3)某学习小组用“间接碘量法”测定含有CuCl2•2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36g试样溶于水,加入过量KI固体,充分反应,生成白色CuI沉淀.过滤后,用0.100 0mol•L-1 Na2S2O3标准溶液滴定所得滤液,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL.
①可选用淀粉作滴定指示剂,滴定终点的现象是蓝色变为无色,且在半分钟内无变化.
②CuCl2溶液与KI反应的离子方程式为2Cu2++4I-=2CuI↓+I2.
③该试样中CuCl2•2H2O的质量百分数为95.0%.
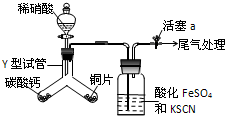 (1)为探究铜与稀硝酸反应的气态产物中是否含NO2,进行如下实验.
(1)为探究铜与稀硝酸反应的气态产物中是否含NO2,进行如下实验.