题目内容
18.下列电子式正确的是( )| A. | H2O2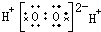 | B. | CCl4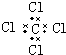 | C. | MgCl2 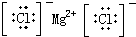 | D. | NaOH 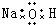 |
分析 首先判断单质或化合物的类型,离子化合物阴离子带电荷且用“[]”,共价化合物不带电荷,注意各原子或离子满足稳定结构.
解答 解:A、双氧水为共价化合物,分子中存在两个氧氢键和一个O-O键,双氧水的电子式为: ,故A错误;
,故A错误;
B、CCl4是共价化合物,碳原子分别与4个氯原子通过一对共用电子对结合,CCl4电子式为 ,故B错误;
,故B错误;
C、氯化镁为离子化合物,化学式中存在阴阳离子,其电子式中需要标出阴阳离子所带电荷,氯化镁的电子式为: ,故C正确;
,故C正确;
D、氢氧化钠属于离子化合物,电子式中需要标出阴阳离子所带电荷,钠离子直接用离子符号表示,氢氧根离子需要标出最外层电子,氢氧化钠的电子式为: 故D错误,故选C.
故D错误,故选C.
点评 本题考查了电子式的书写,题目难度中等,注意掌握电子式的概念及表示方法,明确离子化合物与共价化合物的电子式的表示方法及区别.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.据某科学杂志报道,国外发现了一种新的球形分子,它的分子式为C60Si60,其分子结构好似中国传统工艺品“镂雕”,经测定其中包含C60,也有Si60结构.下列叙述不正确的是( )
| A. | 该物质的熔点不会很高、硬度不会很大 | |
| B. | 该物质形成的晶体属于分子晶体 | |
| C. | 该物质分子中Si60被包裹在C60里面 | |
| D. | 该物质的相对分子质量为2400 |
9.下列各组元素性质或原子结构递变情况错误的是( )
| A. | Li、Be、B原子最外层电子数依次增多 | |
| B. | P、S、Cl元素最高正化合价依次增大 | |
| C. | N、O、F原子半径依次增大 | |
| D. | Na、K、Rb的电子层数依次增多 |
6.能鉴别CO2和SO2的试剂是( )
| A. | 紫色石蕊试液 | B. | 氯化钡溶液 | ||
| C. | 酸性高锰酸钾溶液 | D. | 澄清石灰水 |
13.据报道,在40GPa高压下,用激光器加热到1800K,科学家已成功合成出CO2原子晶体,下列有关这种CO2晶体推断正确的是( )
| A. | 易液化,可用作制冷材料 | |
| B. | CO2晶体中,每个C原子周围结合2个O原子,每个O原子跟1个C原子结合 | |
| C. | 硬度很大,可用作耐磨材料 | |
| D. | 在一定条件下,CO2分子晶体转化为原子晶体是物理变化 |
10.有机物CH2=CH-CH2-CH(OH)-COOH可发生下列反应中的哪几类( )
(1)使溴水褪色 (2)使高锰酸钾溶液褪色 (3)与钠反应 (4)加聚反应
(5)酯化反应 (6)水解反应 (7)取代反应.
(1)使溴水褪色 (2)使高锰酸钾溶液褪色 (3)与钠反应 (4)加聚反应
(5)酯化反应 (6)水解反应 (7)取代反应.
| A. | 除(7)外都可以 | B. | 除(6)外都可以 | C. | (1)(2)(3)(7) | D. | (1)(2)(3)(5) |
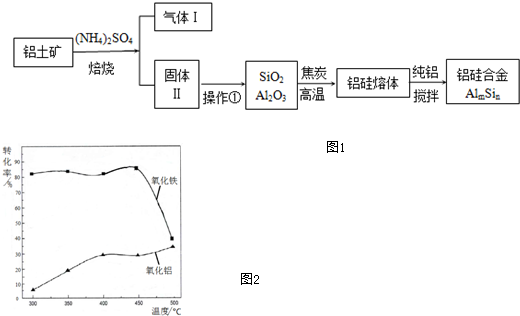
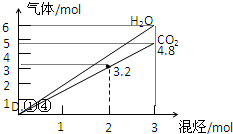 两种气态烃组成的混合气体完全燃烧后得到CO2和H2O的物质的量随混合烃的总物质的量的变化如图所示,
两种气态烃组成的混合气体完全燃烧后得到CO2和H2O的物质的量随混合烃的总物质的量的变化如图所示,