题目内容
8.氯吡格雷(clopidogrel,1)是一种用于抑制血小板聚集的药物,根据原料的不同,该药物的合成路线通常有两条,其中以2氯苯甲醛为原料的合成路线如下: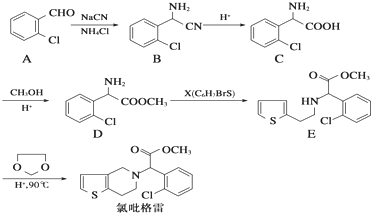 ,
,(1)分子D中的非含氧官能团名称为氨基、氯原子.
(2)D→E的反应类型是取代反应.
(3)X的结构简式为
 .
.(4)分子C可在一定条件下反应生成一种含有3个六元环的产物,写出该反应的化学方程式
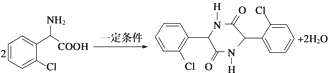 .
.(5)A的属于芳香族化合物的所有同分异构体(不包括A)有3种.
(6)已知:
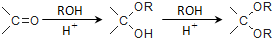 ,则由乙醇、甲醇为有机原料制备化合物
,则由乙醇、甲醇为有机原料制备化合物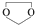 ,需要经历的反应类型有①②③④(填写编号).①加成反应 ②消去反应 ③取代反应 ④氧化反应 ⑤还原反应,写出制备化合物
,需要经历的反应类型有①②③④(填写编号).①加成反应 ②消去反应 ③取代反应 ④氧化反应 ⑤还原反应,写出制备化合物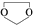 的最后一步反应
的最后一步反应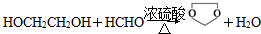 .
.
分析 A反应生成B,B反应生成C,C和甲醇发生酯化反应生成D,D取代反应生成E,根据D、E结构简式结合X分子式知,X结构简式为 ,E发生取代反应生成氯砒格雷,
,E发生取代反应生成氯砒格雷,
(1)分子D中的非含氧官能团名称氨基、氯原子;
(2)D发生取代反应生成E;
(3)根据D、E结合X分子式确定X结构简式;
(4)分子C可在一定条件下发生取代反应生成一种含有3个六元环的产物;
(5)A属于芳香族化合物的所有同分异构体中含有苯环,官能团不变时,改变官能团的位置,若官能团发生变化,侧链为为-COCl;
(6)乙醇发生消去反应生成乙烯,乙烯与溴发生加成反应生成1,2-二溴乙烷,再发生水解反应生成乙二醇,甲醇催化氧化生成HCHO,最后乙二醇与甲醛反应生成 .
.
解答 解:A反应生成B,B反应生成C,C和甲醇发生酯化反应生成D,D取代反应生成E,根据D、E结构简式结合X分子式知,X结构简式为 ,E发生取代反应生成氯砒格雷,
,E发生取代反应生成氯砒格雷,
(1)分子D中的非含氧官能团名称氨基、氯原子,故答案为:氨基、氯原子;
(2)D发生取代反应生成E,其反应类型是取代反应,故答案为:取代;
(3)通过以上分析知,X结构简式为 ,故答案为:
,故答案为: ;
;
(4)分子C可在一定条件下发生取代反应生成一种含有3个六元环的产物,氨基和羧基之间发生取代反应,反应方程式为 ,
,
故答案为: ;
;
(5)属于芳香族化合物的所有同分异构体中含有苯环,官能团不变时,改变官能团的位置,若官能团发生变化,侧链为为-COCl,A属于芳香族化合物的所有同分异构体中含有苯环,官能团不变时,改变官能团的位置,若官能团发生变化,侧链为-COCl,符合条件所有的结构简式为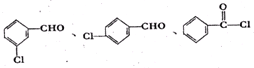 ,
,
故答案为:3;
(6)乙醇发生消去反应生成乙烯,乙烯与溴发生加成反应生成1,2-二溴乙烷,再发生水解反应生成乙二醇,甲醇催化氧化生成HCHO,最后乙二醇与甲醛反应生成 ,涉及的反应类型有:消去反应、加成反应、氧化反应、取代反应,最后一步反应方程式为:
,涉及的反应类型有:消去反应、加成反应、氧化反应、取代反应,最后一步反应方程式为: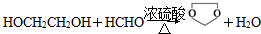 ,
,
故答案为:①②③④;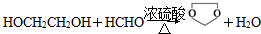 .
.
点评 本题考查有机物合成,侧重考查学生分析推断及知识迁移能力,为高考高频点,能根据流程图中结构简式变化方式判断反应类型,难点是合成路线的设计,根据反应物及目标产物结合有机物中官能团及其性质设计合成路线即可,题目难度中等.

| A. | 正戊烷<异戊烷<新戊烷 | B. | 正戊烷>新戊烷>异戊烷 | ||
| C. | 邻二甲苯>间二甲苯>对二甲苯 | D. | 邻二甲苯<间二甲苯<对二甲苯 |
 氨气是生产化肥、硝酸等的重要原料,围绕合成氨人们进行了一系列的研究
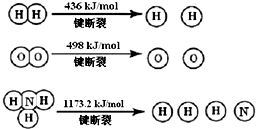
氨气是生产化肥、硝酸等的重要原料,围绕合成氨人们进行了一系列的研究(1)氢气既能与氮气又能与氧气发生反应,但是反应的条件却不相同.已知:
2H2(g)+O2(g)=2H2O (g)△H=-483.6kJ/mol
3H2 (g)+N2(g) 2NH3(g)△H=-92.4kJ/mol
计算断裂1mol N≡N键需要能量946kJ,氮气分子中化学键比氧气分子中的化学键键强(填“强”或“弱”),因此氢气与二者反应的条件不同.
(2)固氮是科学家致力研究的重要课题.自然界中存在天然的大气固氮过程:N2(g)+O2(g)=2NO (g)△H=+180.8kJ/mol,工业合成氨则是人工固氮.分析两种固氮反应的平衡常数,下列结论正确的是BC.
| 反应 | 大气固氮 | 工业固氮 | ||||
| 温度/℃ | 27 | 2000 | 25 | 350 | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 5×108 | 1.847 | 0.507 | 0.152 |
B.人类大规模模拟大气固氮是无意义的
C.工业固氮温度越低,氮气与氢气反应越完全
D.K越大说明合成氨反应的速率越大.
| A. | 分液漏斗中液体的总体积不得超过其容量的2/3 | |
| B. | 萃取时,用右手压住分液漏斗的玻璃塞,左手握住旋塞,将分液漏斗倒过来用力震荡 | |
| C. | 分液漏斗的检漏只需检查旋塞处是否漏水即可 | |
| D. | 课本中测定中和热实验的装置,用铜制环形搅棒代替玻璃环形搅棒更耐用 |
| A. | 一个${\;}_{88}^{226}$Ra原子中含有138个中子 | |
| B. | Ra元素位于元素周期表中第六周期ⅡA族 | |
| C. | Ra不能和冷水反应置换氢气 | |
| D. | Ra(OH)2是一种两性氢氧化物 |