题目内容
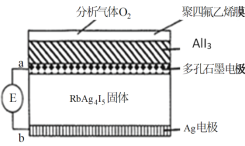
【题目】某测定O2含量的传感器工作原理如图所示。O2通过聚四氟乙烯膜进入传感器只与AlI3反应生成Al2O3和I2,RbAg4I5固体只传导Ag+,E为电位计。下列说法错误的是
A.电子由a极移动到b极
B.RbAg4I5质量不发生变化
C.b极的电极反应式为:Ag+I--e-=AgI
D.该传感器协同总反应方程式为:3O2+4AlI3+12Ag=2Al2O3+12AgI
【答案】AC
【解析】
由图可知,传感器中发生4AlI3+3O2=2Al2O3+6I2,然后生成的碘在多孔石墨电极上被氧化成Iˉ,所以a极为正极,得电子发生还原反应,b电极为负极,Ag失电子发生氧化反应。
A.原电池中电子经导线由负极流向正极,即从b极移动到a极,故A错误;
B.放电过程中负极Ag失电子发生氧化反应生成Ag+进入RbAg4I5固体,根据电荷守恒可知固体中同时有等量的Ag+流入正极,所以RbAg4I5质量不发生变化,故B正确;
C.RbAg4I5固体只传导Ag+,所以碘离子无法到达b极和Ag+反应生成AgI,所以b极的电极反应式为Ag-eˉ=Ag+,故C错误;
D.传感器中发生4AlI3+3O2=2Al2O3+6I2,正极碘被氧化成碘离子后和银离子结合生成AgI,电极反应式为I2+2Ag++2e-=2AgI,负极反应为Ag-eˉ=Ag+,所以协同总反应为:3O2+4AlI3+12Ag=2Al2O3+12AgI,故D正确;
故答案为AC。

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目