题目内容
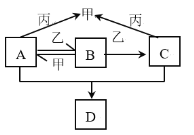
【题目】X、Y、Z、W为原子序数依次增大的短周期主族元素,只有W为金属元素。甲、乙、丙分别为X、Z、W三种元素所对应的单质。A、B、C、D均为由X、Y、Z三种元素组成的化合物,化合物B的稀溶液常用于保存动物标本。它们的转化关系如图所示。下列说法错误的是
A.X与Z可组成非极性分子
B.原子半径大小关系是:r(X)<r(Z)<r(Y)<r(W)
C.四种化合物中B的沸点最低
D.四种化合物中Y原子的杂化方式有2种
【答案】A
【解析】
由“化合物B的稀溶液常用于保存动物标本”,可确定B为HCHO,则X、Y、Z分别为H、C、O;由“甲、乙、丙分别为X、Z、W三种元素所对应的单质”,可确定甲、乙分别为H2、O2;由转化关系图,可确定A为CH3OH,C为HCOOH,D为HCOOCH3;由A与丙反应可生成甲,可确定丙为Na,即W为Na。
A.X与Z分别为H和O,二者可组成H2O、H2O2,它们都是极性分子,A错误;
B.H的核外只有1个电子层,半径最小,C、O同周期,C在O的左边,原子半径C比O大,Na的电子层数最多,半径最大,所以原子半径大小关系是:r(H)<r(O)<r(C)<r(Na),B正确;
C.四种化合物中,B为HCHO,常温下呈气态,而另三种物质都呈液态,所以B的沸点最低,C正确;
D.四种化合物中Y原子的杂化方式有:含-CH3的物质,碳原子发生sp3杂化,含碳氧双键的物质,碳氧双键中碳原子发生sp2杂化,D正确;
故选A。

【题目】在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下[已知N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ·mol-1],下列说法正确的是( )
2NH3(g) ΔH=-92.4 kJ·mol-1],下列说法正确的是( )
容器 | 甲 | 乙 | 丙 |
反应物投入量 | 1 mol N2、 3 mol H2 | 2 mol NH3 | 4 mol NH3 |
NH3的浓 度/mol·L-1 | c1 | c2 | c3 |
反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
体系压强(Pa) | p1 | p2 | p3 |
反应物转化率 | α1 | α2 | α3 |
A. 2c1>c3B. α1+α3<1C. 2p2<p3D. a+b>92.4