题目内容
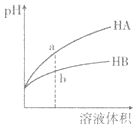
【题目】常温下,将0.025molBaSO4粉末置于盛有蒸馏水的烧杯中形成1L 悬浊液,然后向烧杯中加入Na2CO3固体(忽略溶液体积的变化)并充分搅拌。加入Na2CO3固体的过程中溶液中几种离子的浓度变化曲线如图所示,下列说法中正确的是( )
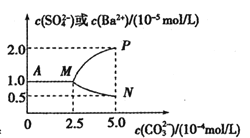
A.常温下,Ksp(BaSO4)=2.5×10-9
B.BaSO4中的溶解度、Ksp均比在BaCl2溶液中的大
C.若要使BaSO4全部转化为BaCO3至少要加入0.65mol Na2CO3
D.BaSO4恰好全部转化为BaCO3时,溶液中离子浓度大小关系为:c(![]() )>c(
)>c(![]() )>c(Ba2+)>c(OH-)
)>c(Ba2+)>c(OH-)
【答案】C
【解析】
A. 常温下,没有加入碳酸钠时,c(Ba2+)=c(![]() )=1×10-5mol/L,
)=1×10-5mol/L,![]() ,A错误;
,A错误;
B. BaSO4在BaCl2溶液中由于Ba2+的存在,使沉淀溶解平衡逆向移动,因此BaSO4在BaCl2溶液中的溶解度比在水中小,Ksp只随温度的改变而改变,无论在水中还是BaCl2溶液中,Ksp值是不变的,B错误;
C. 根据图像:![]() ,当c(
,当c(![]() )=2.5×10-4mol/L时开始形成BaCO3沉淀,
)=2.5×10-4mol/L时开始形成BaCO3沉淀,![]() ,
,![]() 反应的平衡常数为:
反应的平衡常数为:![]() ,若使0.025mol BaSO4全部转化为BaCO3,则反应消耗0.025mol
,若使0.025mol BaSO4全部转化为BaCO3,则反应消耗0.025mol![]() 、生成0.025mol
、生成0.025mol![]() ,反应达到平衡时,
,反应达到平衡时,![]() ,解得c(
,解得c(![]() )=0.625mol/L,则至少需要Na2CO3的物质的量为:0.625mol/L×1L+0.025mol=0.65mol,C正确;
)=0.625mol/L,则至少需要Na2CO3的物质的量为:0.625mol/L×1L+0.025mol=0.65mol,C正确;
D. 根据C项计算,当BaSO4恰好全部转化为BaCO3时,c(![]() )=0.625mol/L,c(
)=0.625mol/L,c(![]() )=0.025mol/L,c(Ba2+)=2.5×10-9÷0.625=4×10-9(mol/L),由于
)=0.025mol/L,c(Ba2+)=2.5×10-9÷0.625=4×10-9(mol/L),由于![]() 水解溶液呈碱性,离子浓度大小关系为:c(
水解溶液呈碱性,离子浓度大小关系为:c(![]() )>c(
)>c(![]() )>c(OH-)>c(Ba2+),D错误;
)>c(OH-)>c(Ba2+),D错误;
故答案为:C。

 阅读快车系列答案
阅读快车系列答案【题目】一定温度下,在3个1.0 L的恒容密闭容器中分别进行反应2X(g)+Y(g)![]() Z(g) ΔH,达到平衡。相关数据如下表。
Z(g) ΔH,达到平衡。相关数据如下表。
容器 | 温度/K | 物质的起始浓度/ mol·L-1 | 物质的平衡浓度/ mol·L-1 | ||
c(X) | c(Y) | c(Z) | c(Z) | ||
I | 400 | 0.20 | 0.10 | 0 | 0.080 |
II | 400 | 0.40 | 0.20 | 0 | a |
III | 500 | 0.20 | 0.10 | 0 | 0.025 |
下列说法不正确的是
A. 平衡时,X的转化率:II>I
B. 平衡常数:K(II)>K(I)
C. 达到平衡所需时间:III<I
D. 反应的ΔH<0
【题目】下列实验“操作和现象”与“结论”对应且正确的是( )
操作和现象 | 结论 | |
A | 向盛有浓硫酸的试管中加入铜片,铜片很快开始溶解,并放出刺激性气味的气体 | 浓硫酸具有强氧化性 |
B | 向两支盛有KI3的溶液的试管中,分别滴加淀粉溶液和硝酸银溶液,前者溶液变蓝,后者有黄色沉淀 | KI3溶液中存在平衡:I |
C | 向一定量的硝酸银溶液中先滴加KCl溶液,再滴加KI溶液,先出现白色沉淀,后出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
D | 室温下,用pH试纸分别测定浓度为0.1mol/LNaClO溶液和0.1mol/LCH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
A.AB.BC.CD.D