题目内容
【题目】化学兴趣A组的同学们利用废硫酸溶液制备K2SO4晶体,设计流程如下图所示:
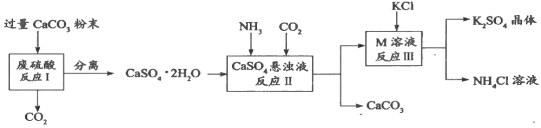
(1)写出反应Ⅰ的化学方程式:______________________。
(2)反应Ⅱ生成了一种可用作肥料的物质M,M的化学式为_________________。
(3)上述流程中可循环使用的物质有CO2和_________(填化学式)。
(4)反应Ⅲ中相关物质在25℃时的溶解度如下表。
物质 |
|
|
|
|
溶解度/g | 34.0 | 11.1 | 37.2 | 19.5 |
反应Ⅲ在常温下(25℃)能实现的原因是_________________________。
(5)不用水而用饱和K2SO4溶液洗涤反应Ⅲ所得晶体的原因是_____________;为了检验此晶体是否洗涤干净,取最后一次洗涤液于试管中,先加入过量的_______(选填字母),振荡、静置, 再向上层清液中滴加_______(选填字母),观察现象即可判断该晶体是否洗涤干净。
A. AgNO3溶液 B. BaCl2溶液 C. Ba(NO3)2溶液 D .Ba(OH)2溶液 E. NaOH溶液
【答案】CaCO3+H2SO4=CaSO4+CO2↑+H2O (NH4)2SO4 CaCO3 此时K2SO4的溶解度很小 减少K2SO4的溶解(而造成的损耗) C A
【解析】
根据给出的转化关系对应的过程分析每个对应的问题,或者直接分析每个问题,从给出的信息中找对应的信息。在判断物质成分时,要结合物质的溶解度大小分析,在判断晶体是否洗涤干净时,要考虑到可能混有的杂质成分及检验的先后顺序,选择合适的催化剂。
(1)反应I是碳酸钙和硫酸反应生成硫酸钙和水以及二氧化碳,该反应的化学方程式为:CaCO3+H2SO4=CaSO4+H2O+CO2↑。
(2)NH3、CO2、CaSO4在溶液中发生反应Ⅱ生成CaCO3、(NH4)2SO4,农作物生长需要大量氮肥,一种可用作氮肥的物质M是(NH4)2SO4,而M和氯化钾反应生成了硫酸钾和氯化铵,根据质量守恒定律以及复分解反应特点,M的化学式为(NH4)2SO4。
(3)在上述流程中碳酸钙开始反应物后来是生成物,所以碳酸钙可以循环利用。而二氧化碳开始是生成物,后来是反应物,也可以循环利用。故可循环使用的物质的化学式为CO2和CaCO3。
(4)根据相关物质在25℃时的溶解度表可知,在该温度下,硫酸钾在该温度下溶解度很小。反应Ⅲ在常温下(25℃)能实现的原因是硫酸钾在该温度下溶解度很小,相对其他物质可以视为不溶,符合复分解反应的条件。
(5)不用水而用饱和K2SO4溶液洗涤反应Ⅲ所得晶体的目的是减少硫酸钾因洗涤造成的损失;为了检验此晶体是否洗涤干净,即检验饱和的硫酸钾溶液中是否含有氯化铵,也就是在有SO42-干扰的情况下检验Cl-,需要先除去SO42-,在排除SO42-的干扰后再进行Cl-检验。因此具体操作为:最后一次洗涤液于试管中,先加入过量的硝酸钡(不能用氯化钡溶液,防止引入氯离子造成后期干扰),振荡、静置,再向上层清液中滴加硝酸银溶液,若无白色沉淀,就证明沉淀洗涤干净,否则未洗涤干净,故合理选项是C、A。

 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案【题目】如表所示为元素周期表的一部分,参照元素①~⑨在表中的位置,请回答下列问题:
ⅠA | 0 | |||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ⑧ | ⑨ | ② | ③ | ||||
3 | ④ | ⑤ | ⑥ | ⑦ | ||||
(1)③、④、⑦的原子半径由大到小的顺序是________(用元素符号表示)。
(2)下列事实能说明元素②的非金属性比元素⑥的非金属性强的是________(填字母)。
A.②的单质与元素⑥的简单氢化物溶液反应,溶液变浑浊
B.在氧化还原反应中,1mol②单质比1mol⑥单质得电子多
C.②和⑥两元素的简单氢化物受热分解,前者的分解温度高
(3)①、②两种元素按原子个数之比为1∶1组成的常见液态化合物,在酸性溶液中能将Fe2+氧化,写出该反应的离子方程式: ____。
(4)已知周期表中存在对角相似规则,如铍(Be)与铝化学性质相似,⑧的氧化物、氢氧化物也有两性,写出⑧的氢氧化物与④的最高价氧化物的水化物反应的化学方程式:________。
(5)已知W+X=Y+Z(反应需要加热),W、X、Y、Z分别是由①②⑨三种元素形成的四种10电子粒子(W、X为离子,Y、Z为分子),写出该离子方程式___________