题目内容
18.短周期主族元素X、Y、Z、W的原子序数依次增大,已知X、Y、Z+、W各微粒最外层电子数与其电子层数之比值依次为2、3、4、2,下列有关这四种元素叙述正确的是( )| A. | Y与X、Z、W分别能形成两种化合物 | |
| B. | Z与W形成的Z2W型化合物在水溶液中Z+离子与W2-离子个数比为2:1 | |
| C. | Y、Z、W不可能形成水溶液呈碱性的化合物 | |
| D. | 化合物X Y2、X YW、X W2随着共价键的键长逐渐增大,熔沸点逐渐降低 |
分析 短周期元素X、Y、Z、W原子序数依次增大,且X、Y、Z+、W的最外层电子数与其电子层数的比值依次为2、3、4、2,Z+的电子层数为2,最外层电子数为8,所以Z的质子数为2+8+1=11,所以Z为Na;结合原子序数可知,X的电子层数为2,最外层电子数为4,所以X为C;Y的电子层数为2,最外层电子数为6,所以Y为O;W的电子层数为3,最外层电子数为6,所以W为S,然后结合元素及其化合物的性质来解答.
解答 解:短周期元素X、Y、Z、W原子序数依次增大,且X、Y、Z+、W的最外层电子数与其电子层数的比值依次为2、3、4、2,Z+的电子层数为2,最外层电子数为8,
所以Z的质子数为2+8+1=11,所以Z为Na;
结合原子序数可知,X的电子层数为2,最外层电子数为4,所以X为C;
Y的电子层数为2,最外层电子数为6,所以Y为O;
W的电子层数为3,最外层电子数为6,所以W为S,
A.O和C形成CO、CO2,O和Na形成Na2O、Na2O2,O和S形成SO2、SO3,故A正确;
B.Z与W形成Na2S,在水溶液中S2-离子水解,故溶液Na+离子与S2-离子个数比大于2:1,故B错误;
C.Y、Z、W可能形成硫酸钠、亚硫酸钠,亚硫酸钠溶液呈碱性,故C错误;
D.CO2、COS、CS2共价键的键长逐渐增大,都属于分子晶体,相对分子质量增大,熔沸点增大,故D错误,
故选:A.
点评 本题考查原子结构和元素周期律,元素的推断是解答本题的关系,注意短周期不考虑稀有气体时电子层为2或3即可解答,难度中等.

练习册系列答案
相关题目
8.下列化学用语表达正确的是( )
| A. | 环已烷的结构简式 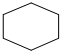 | B. | C2H4的球棍模型 | ||
| C. | 四氯化碳的电子式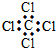 | D. | 苯的分子式 |
9.有关化学用语正确的是( )
| A. | 乙烯的实验式C2H4 | B. | 乙醇的结构简式C2H6O | ||
| C. | 四氯化碳的电子式: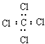 | D. | 3,3,4-三甲基已烷的分子式C9H20 |
3.T、X、Y、Z、Q、R、W为周期表前四周期元素,原子序数依次递增,其中某些元素的相关信息如下表:
(1)X、Y、Q三种元素的电负性由大到小的顺序是N>C>Na(用元素符号表示).
(2)X与Y原子结合形成的X3Y4晶体,晶体结构与金刚石类似,则X3Y4晶体的熔点比金刚石要高(填“高”、“低”).
(3)W2+的核外电子排布式为[Ar]3d9.元素W与人体分泌物中的盐酸以及空气反应可生成超氧酸:W+HCl+O2=WCl+HO2,HO2 (超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性.下列说法或表示错误的是C
A.氧化剂是O2 B.HO2在碱中不能稳定存在
C.氧化产物是HO2 D.1molW参加反应有1mol电子发生转移
(4)X、Y、Z分别与氢元素可以构成A、B、C、D等多种粒子.其中A、B、C均为10电子微粒,D为18电子微粒.A为5原子核的+1价阳离子,则A+的中心原子杂化方式为sp3.B为4原子核的+1价阳离子,则B+电子式为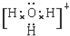 .C为4个原子核构成的分子,则与C互为等电子体的分子可以是
.C为4个原子核构成的分子,则与C互为等电子体的分子可以是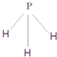 (写结构式).D分子中两元素的原子个数之比为1:1,则D为极性(填“极性”或“非极性”)分子.某双原子单质分子E也为18电子微粒,E与水的反应的化学方程式为2F2+2H2O=4HF+O2.
(写结构式).D分子中两元素的原子个数之比为1:1,则D为极性(填“极性”或“非极性”)分子.某双原子单质分子E也为18电子微粒,E与水的反应的化学方程式为2F2+2H2O=4HF+O2.
(5)已知25℃、101kPa条件下:
4R(s)+3Z2(g)═2R2Z3(s)△H=-2835.9kJ/mol
4R(s)+2Z3(g)═2R2Z3(s)△H=-3119.1kJ/mol
则16g Z2(g)完全转化为Z3(g)的△H=+47.4 kJ/mol.
| 元素 | 相关信息 |
| T | T原子所处的周期数、族序数分别与其原子序数相等 |
| X | X的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子数相同 |
| Z | Z的基态原子价电子排布为ns2npn+2 |
| Q | 在该元素所在周期中,Q的基态原子的第一电离能最小 |
| R | 3p能级上有1个电子 |
| W | W的一种核素的质量数为65,中子数为36 |
(2)X与Y原子结合形成的X3Y4晶体,晶体结构与金刚石类似,则X3Y4晶体的熔点比金刚石要高(填“高”、“低”).
(3)W2+的核外电子排布式为[Ar]3d9.元素W与人体分泌物中的盐酸以及空气反应可生成超氧酸:W+HCl+O2=WCl+HO2,HO2 (超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性.下列说法或表示错误的是C
A.氧化剂是O2 B.HO2在碱中不能稳定存在
C.氧化产物是HO2 D.1molW参加反应有1mol电子发生转移
(4)X、Y、Z分别与氢元素可以构成A、B、C、D等多种粒子.其中A、B、C均为10电子微粒,D为18电子微粒.A为5原子核的+1价阳离子,则A+的中心原子杂化方式为sp3.B为4原子核的+1价阳离子,则B+电子式为
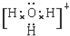 .C为4个原子核构成的分子,则与C互为等电子体的分子可以是
.C为4个原子核构成的分子,则与C互为等电子体的分子可以是 (写结构式).D分子中两元素的原子个数之比为1:1,则D为极性(填“极性”或“非极性”)分子.某双原子单质分子E也为18电子微粒,E与水的反应的化学方程式为2F2+2H2O=4HF+O2.
(写结构式).D分子中两元素的原子个数之比为1:1,则D为极性(填“极性”或“非极性”)分子.某双原子单质分子E也为18电子微粒,E与水的反应的化学方程式为2F2+2H2O=4HF+O2.(5)已知25℃、101kPa条件下:
4R(s)+3Z2(g)═2R2Z3(s)△H=-2835.9kJ/mol
4R(s)+2Z3(g)═2R2Z3(s)△H=-3119.1kJ/mol
则16g Z2(g)完全转化为Z3(g)的△H=+47.4 kJ/mol.
10.如图是常见四种有机物的比例模型示意图.下列说法正确的是( )
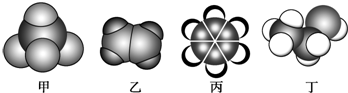

| A. | 甲能使酸性高锰酸钾溶液褪色 | |
| B. | 乙可与溴水发生加成反应使溴水褪色 | |
| C. | 丙与溴水可以发生取代反应 | |
| D. | 丁在稀硫酸作用下可与乙酸发生取代反应 |
7.已知aXm+、bYn-、cZm-(m>n)三中离子具有相同的电子层结构,下列关系正确的是( )
| A. | 原子序数:a>b>c | B. | 离子半径:Yn->Zm- | ||
| C. | a-b=m-n | D. | 原子核外最外层电子数:X>Y>Z |
 .
.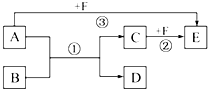 已知:A、B、C、D、E、F是中学化学教材中六种常见的物质,它们之间有如图所示的相互转化关系(反应条件及部分产物未标出).请回答下列问题:
已知:A、B、C、D、E、F是中学化学教材中六种常见的物质,它们之间有如图所示的相互转化关系(反应条件及部分产物未标出).请回答下列问题: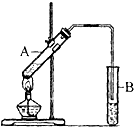 乙酸是白醋中的主要成分.
乙酸是白醋中的主要成分.