题目内容
合金在生产及科研中具有广泛的应用.下列物质不属于合金的是( )
| A、铝箔 | B、青铜 | C、铁板 | D、不锈钢 |
考点:合金的概念及其重要应用
专题:元素及其化合物
分析:合金是指在一种金属中加热熔合其它金属或非金属而形成的具有金属特性的物质.合金概念有三个特点:①一定是混合物;②合金中各成分都是以单质形式存在;③合金中至少有一种金属.
解答:
解:A、铝箔是铝,属于单质,故A选;
B、青铜中含有铜、锡、铅,属于合金,故B不选;
C、铁板中含有碳、铁,属于合金,故C不选;
D、不锈钢中含有铁、铬、碳,属于合金,故D不选.
故选A.
B、青铜中含有铜、锡、铅,属于合金,故B不选;
C、铁板中含有碳、铁,属于合金,故C不选;
D、不锈钢中含有铁、铬、碳,属于合金,故D不选.
故选A.
点评:本题考查了合金的判断,难度不大,注意合金的成分不都是金属,也可能含有非金属,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
如表代表周期表中的几种短周期元素,下列说法中正确的是( )
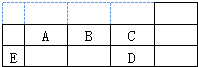

| A、C、D的氢化物沸点D比C高 |
| B、第一电离能A、B、C依此增大 |
| C、A、B、C中电负性最大的A |
| D、五种元素中,最高价氧化物对应的水化物酸性最强的是D |
NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、非标准状况下,1mol任何气体的体积不可能为22.4L |
| B、常温常压下,0.2mol Na2O2与足量H2O反应,转移电子的数目为0.2NA |
| C、标准状况下,NA个水分子所占的体积为22.4L |
| D、常温常压下,0.2mol Na2O2含有0.4mol阴离子 |
下列说法或表达正确的是( )
| A、强电解质溶液的导电能力一定比弱电解质溶液强 | ||
B、S2-的结构示意图: | ||
C、质子数为53,中子数为78的碘原子:
| ||
| D、干冰和液氯都是非电解质 |
Fe与HNO3反应随温度和HNO3的浓度不同而产物不同.已知0.2mol HNO3作氧化剂时,恰好把0.2mol Fe氧化,则HNO3可能被还原成( )
| A、NH4+ |
| B、NO2 |
| C、NO |
| D、N2O3 |
铜既不溶于稀硫酸,也不溶于KNO3溶液,但可溶于二者的混合液.现将1.92g Cu放入足量的稀硫酸中,若要使铜完全溶解,理论上至少应加入KNO3晶体的物质的量为( )
| A、0.08mol |
| B、0.06mol |
| C、0.045mol |
| D、0.02mol |