题目内容
下列说法或表达正确的是( )
| A、强电解质溶液的导电能力一定比弱电解质溶液强 | ||
B、S2-的结构示意图: | ||
C、质子数为53,中子数为78的碘原子:
| ||
| D、干冰和液氯都是非电解质 |
考点:强电解质和弱电解质的概念,核素,原子结构示意图,电解质与非电解质
专题:物质的组成专题,电离平衡与溶液的pH专题
分析:A.溶液的导电能力与溶液中离子浓度成正比,与电解质的强弱无关;
B.硫离子核内质子数为16,核外电子数为18;
C.原子符号的左上角的数字是质量数,左下角的数字是质子数;
D.非电解质:在熔融状态和水溶液中都不能导电的化合物.
B.硫离子核内质子数为16,核外电子数为18;
C.原子符号的左上角的数字是质量数,左下角的数字是质子数;
D.非电解质:在熔融状态和水溶液中都不能导电的化合物.
解答:
解:A.溶液的导电能力与溶液中离子浓度成正比,与电解质的强弱无关,强电解质溶液的导电能力不一定比弱电解质溶液强,故A错误;
B.硫离子核内质子数为16,核外电子数为18,故结构示意图为: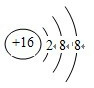 故B错误;
故B错误;
C.质子数为53,中子数为78的碘原子的符号为:53131I,故C正确;
D.干冰是二氧化碳,本身不能电离,是非电解质;液氯是单质,既不是电解质也不是非电解质,故D错误,
故选C.
B.硫离子核内质子数为16,核外电子数为18,故结构示意图为:
 故B错误;
故B错误;C.质子数为53,中子数为78的碘原子的符号为:53131I,故C正确;
D.干冰是二氧化碳,本身不能电离,是非电解质;液氯是单质,既不是电解质也不是非电解质,故D错误,
故选C.
点评:本题考查溶液的导电能力,非电解质的判断,离子结构示意图和原子符号等,为高频考点,难度不大.把握化学用语的规范应用是解答的关键.

练习册系列答案
相关题目
下列物质既可以通过金属与氯气反应制得,又可以通过金属与稀盐酸反应制得( )
| A、FeCl2 |
| B、FeCl3 |
| C、CuCl2 |
| D、AlCl3 |
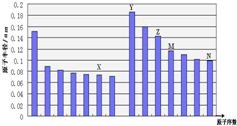 如图是部分短周期元素原子半径与原子序数的关系图,下列说法不正确的是( )
如图是部分短周期元素原子半径与原子序数的关系图,下列说法不正确的是( )| A、N、Z两种元素的离子半径相比前者较大 |
| B、M、N两种元素的气态氢化物的稳定性相比后者较强 |
| C、X与M两种元素组成的化合物能与水反应生成相应的酸 |
| D、工业上常用电解Y和N形成的化合物的熔融态制取Y的单质 |
A2、B2、C2三种单质和它们的离子间能发生如下反应:
①2A-+C2→2C-+A2;
②2C-+B2→2B-+C2;
③2X-+C2→2C-+X2;
则下列判断中错误的是( )
①2A-+C2→2C-+A2;
②2C-+B2→2B-+C2;
③2X-+C2→2C-+X2;
则下列判断中错误的是( )
| A、氧化性最强:B2 |
| B、还原性最强:X- |
| C、X2与B-一定不能发生反应 |
| D、X2与A-一定不能发生反应 |
下列物质的分类合理的是( )
| A、酸:H2S、H2O、H2SO4、H2CO3 |
| B、碱:NaOH、KOH、Ba(OH)2、Cu2(OH)2CO3 |
| C、铵盐:NH4Cl、NH4NO3、(NH4)2SO4、NH3?H2O |
| D、氧化物:CO2、NO、SO2、H2O |
合金在生产及科研中具有广泛的应用.下列物质不属于合金的是( )
| A、铝箔 | B、青铜 | C、铁板 | D、不锈钢 |