题目内容
NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、非标准状况下,1mol任何气体的体积不可能为22.4L |
| B、常温常压下,0.2mol Na2O2与足量H2O反应,转移电子的数目为0.2NA |
| C、标准状况下,NA个水分子所占的体积为22.4L |
| D、常温常压下,0.2mol Na2O2含有0.4mol阴离子 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.由于温度和压强影响气体的体积,所以不是标况下,改变温度和压强后,1mol气体的体积可能为22.4L;
B.过氧化钠中氧元素为-1价,根据0.2mol过氧化钠完全反应生成氧气的物质的量计算出转移的电子数;
C.标准状况下,水的状态不是气体,不能使用标况下的气体摩尔体积计算水的体积;
D.过氧化钠中含有的阴离子为过氧根离子,0.2mol过氧化钠中含有0.2mol阴离子.
B.过氧化钠中氧元素为-1价,根据0.2mol过氧化钠完全反应生成氧气的物质的量计算出转移的电子数;
C.标准状况下,水的状态不是气体,不能使用标况下的气体摩尔体积计算水的体积;
D.过氧化钠中含有的阴离子为过氧根离子,0.2mol过氧化钠中含有0.2mol阴离子.
解答:
解:A.标准状况下,1mol气体的体积约为22.4L,如果同时升高温度、减小压强,气体的体积还可能为22.4L,故A错误;
B.0.2mol过氧化钠与足量水完全反应生成0.1mol氧气,转移了0.2mol电子,转移电子的数目为0.2NA,故B正确;
C.标况下,水不是气体,不能使用标况下的气体摩尔体积计算NA个水分子的体积,故C错误;
D.0.2mol过氧化钠中含有0.2mol过氧根阴离子,含有0.2mol阴离子,故D错误;
故选B.
B.0.2mol过氧化钠与足量水完全反应生成0.1mol氧气,转移了0.2mol电子,转移电子的数目为0.2NA,故B正确;
C.标况下,水不是气体,不能使用标况下的气体摩尔体积计算NA个水分子的体积,故C错误;
D.0.2mol过氧化钠中含有0.2mol过氧根阴离子,含有0.2mol阴离子,故D错误;
故选B.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下气体摩尔体积的使用条件,要求学生掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确过氧化钠中阴离子为过氧根离子、氧元素的化合价为-1价.

练习册系列答案
相关题目
某乙醇水溶液的质量分数为w%,物质的量浓度为c mol/L,密度为d g/mL,1Kg这种溶液中含有的乙醇是( )
| A、46C g |
| B、c/d mol |
| C、c mol |
| D、1000dw g |
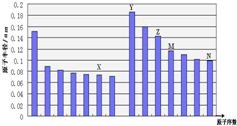 如图是部分短周期元素原子半径与原子序数的关系图,下列说法不正确的是( )
如图是部分短周期元素原子半径与原子序数的关系图,下列说法不正确的是( )| A、N、Z两种元素的离子半径相比前者较大 |
| B、M、N两种元素的气态氢化物的稳定性相比后者较强 |
| C、X与M两种元素组成的化合物能与水反应生成相应的酸 |
| D、工业上常用电解Y和N形成的化合物的熔融态制取Y的单质 |
在下列溶液中,各组离子一定能够大量共存的是( )
| A、使酚酞试液变红的溶液:Na+、Cl-、SO42-、K+ |
| B、使紫色石蕊试液变红的溶液:Fe2+、Mg2+、NO3-、Cl-? |
| C、pH=12的溶液:K+、Mg2+、Cl-、Br- |
| D、碳酸氢钠溶液:K+、SO32-、Cl-、H+ |
A2、B2、C2三种单质和它们的离子间能发生如下反应:
①2A-+C2→2C-+A2;
②2C-+B2→2B-+C2;
③2X-+C2→2C-+X2;
则下列判断中错误的是( )
①2A-+C2→2C-+A2;
②2C-+B2→2B-+C2;
③2X-+C2→2C-+X2;
则下列判断中错误的是( )
| A、氧化性最强:B2 |
| B、还原性最强:X- |
| C、X2与B-一定不能发生反应 |
| D、X2与A-一定不能发生反应 |
合金在生产及科研中具有广泛的应用.下列物质不属于合金的是( )
| A、铝箔 | B、青铜 | C、铁板 | D、不锈钢 |