题目内容
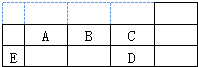
如表代表周期表中的几种短周期元素,下列说法中正确的是( )

| A、C、D的氢化物沸点D比C高 |
| B、第一电离能A、B、C依此增大 |
| C、A、B、C中电负性最大的A |
| D、五种元素中,最高价氧化物对应的水化物酸性最强的是D |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由元素在短周期中的位置,可知A为N元素、B为O氧元素、C为F元素、E为Al、D为Cl,
A.根据HF分子之间存在氢键分析;
B.同周期随原子序数增大,第一电离能呈增大趋势,但N元素原子2p能级为半满稳定状态,第一电离能高于同周期相邻元素;
C.同周期自左而右电负性增大;
D.氟元素没有最高价含氧酸,高氯酸是最强的外界含氧酸.
A.根据HF分子之间存在氢键分析;
B.同周期随原子序数增大,第一电离能呈增大趋势,但N元素原子2p能级为半满稳定状态,第一电离能高于同周期相邻元素;
C.同周期自左而右电负性增大;
D.氟元素没有最高价含氧酸,高氯酸是最强的外界含氧酸.
解答:
解:由元素在短周期中的位置,可知A为N元素、B为O氧元素、C为F元素、E为Al、D为Cl,
A.HF分子之间存在氢键,沸点比较HCl高,故A错误;
B.同周期随原子序数增大,第一电离能呈增大趋势,但N元素原子2p能级容纳3个电子,为半满稳定状态,能量较低,第一电离能高于同周期相邻元素,故第一电离能O<N<F,故B错误;
C.同周期自左而右电负性增大,故电负性F>O>N,故C错误;
D.氟元素没有最高价含氧酸,高氯酸是最强的无机含氧酸,故D正确,
故选D.
A.HF分子之间存在氢键,沸点比较HCl高,故A错误;
B.同周期随原子序数增大,第一电离能呈增大趋势,但N元素原子2p能级容纳3个电子,为半满稳定状态,能量较低,第一电离能高于同周期相邻元素,故第一电离能O<N<F,故B错误;
C.同周期自左而右电负性增大,故电负性F>O>N,故C错误;
D.氟元素没有最高价含氧酸,高氯酸是最强的无机含氧酸,故D正确,
故选D.
点评:本题考查元素周期表与元素周期律,侧重对元素周期律的考查,难度不大,注意整体把握元素周期表的结构.

练习册系列答案
相关题目
下面有关合金说法正确的是( )
| A、现代使用最广泛的合金是铝合金 |
| B、我国使用最早的合金是铁合金 |
| C、合金的熔点比各组分单质大 |
| D、合金的硬度比各组分单质大 |
某乙醇水溶液的质量分数为w%,物质的量浓度为c mol/L,密度为d g/mL,1Kg这种溶液中含有的乙醇是( )
| A、46C g |
| B、c/d mol |
| C、c mol |
| D、1000dw g |
下列物质既可以通过金属与氯气反应制得,又可以通过金属与稀盐酸反应制得( )
| A、FeCl2 |
| B、FeCl3 |
| C、CuCl2 |
| D、AlCl3 |
下列关于卤素单质的叙述,不正确的是( )
| A、单质的颜色随核电荷数的增加逐渐变深 |
| B、随核电荷数的增加单质的氧化性逐渐增强 |
| C、随核电荷数的增加气态氢化物的稳定性逐渐减弱 |
| D、单质的熔沸点随核电荷数的增加逐渐升高 |
下列分子中存在π键的是( )
| A、H2O |
| B、CH4 |
| C、NH3 |
| D、CO2 |
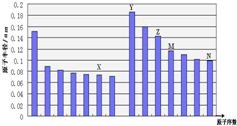 如图是部分短周期元素原子半径与原子序数的关系图,下列说法不正确的是( )
如图是部分短周期元素原子半径与原子序数的关系图,下列说法不正确的是( )| A、N、Z两种元素的离子半径相比前者较大 |
| B、M、N两种元素的气态氢化物的稳定性相比后者较强 |
| C、X与M两种元素组成的化合物能与水反应生成相应的酸 |
| D、工业上常用电解Y和N形成的化合物的熔融态制取Y的单质 |
合金在生产及科研中具有广泛的应用.下列物质不属于合金的是( )
| A、铝箔 | B、青铜 | C、铁板 | D、不锈钢 |