题目内容
15.A、B、C、D、E五种短周期主族元素,它们的原子序数依次增大.已知:A和C、B和D分别位于同主族,且B、D质子数之和是A、C质子数之和的2倍.下列说法正确的是( )| A. | 原子半径的大小顺序:r(B)>r(C)>r(D) | |
| B. | B的简单气态氢化物的热稳定性比D的弱 | |
| C. | E分别与A、C形成的化合物中化学键类型相同 | |
| D. | C的最高价氧化物对应水化物的碱性在同周期中最强 |
分析 有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,A和C、B和D分别位于同主族,假设A是H元素,B的原子序数小于C,则C是Na元素,且B、D质子数之和是A、C质子数之和的2倍,则B是O元素,D是S元素,所以假设成立,E为主族的短周期元素,且原子序数最大,E是Cl元素,结合对应单质化合物的性质以及元素周期率知识解答该题.
解答 解:有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,A和C、B和D分别位于同主族,假设A是H元素,B的原子序数小于C,则C是Na元素,且B、D质子数之和是A、C质子数之和的2倍,则B是O元素,D是S元素,所以假设成立,E为主族的短周期元素,且原子序数最大,E是Cl元素,
A.原子核外电子层数越多,原子半径越大,应为Na>S>O,故A错误;
B.非金属性O>S,非金属性越强,对应的氢化物越稳定,故B错误;
C.E分别与A、C形成的化合物分别为氯化氢、氯化钠,分别为共价化合物和离子化合物,化学键类型不同,故C错误;
D.C为Na,在第三周期中金属性最强,最高价氧化物对应水化物的碱性在同周期中最强,故D正确.
故选D.
点评 本题考查原子结构与元素周期律的关系,为高考常见题型和高频考点,题目难度不大,本题的关键是根据原子结构特点正确推断元素的种类.

练习册系列答案
相关题目
3.下表中a、b、c表示相应仪器中加人的试剂,可用如图装置制取、净化、收集的气体是( )
| 编号 | 气体 | a | b | c | 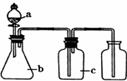 |
| A | NH3 | 浓氨水 | 生石灰 | 碱石灰 | |
| B | CO2 | 盐酸 | 碳酸钙 | 饱和NaHCO3溶液 | |
| C | NO | 稀硝酸 | 铜屑 | H2O | |
| D | Cl2 | 浓盐酸 | 二氧化锰 | 饱和NaCl溶液 |
| A. | A | B. | B | C. | C | D. | D |
10.某有机物的结构简式如图,下列关于该有机物的叙述正确的是( )
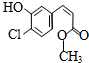

| A. | 该有机物的摩尔质量为200 | |
| B. | 该有机物属于芳香烃 | |
| C. | 该有机物可发生取代、加成、加聚、氧化、还原、消去反应 | |
| D. | 1 mol该有机物在适当条件下,最多可与4mol NaOH和4mol H2反应 |
7.在FeCl3和CuCl2的混合溶液中加入过量铁粉,反应完全后剩余固体的质量大于加入的铁粉质量.已知原混合溶液中FeCl3为0.4mol,则CuCl2的物质的量可能是( )
| A. | 0.2 mol | B. | 0.6 mol | C. | 1.2 mol | D. | 2 mol |
5.短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法不正确的是( )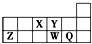

| A. | 离子半径的大小顺序为r(W2-)>r(Q-)>r(Y2-)>r(Z3+) | |
| B. | 元素W的最高价氧化物对应水化物的酸性比Q的强 | |
| C. | 元素X与Q的氢化物化合的产物中既含共价键又含离子键 | |
| D. | X、Z、W、Q四种元素的最高价氧化物对应的水化物均能与强碱反应 |
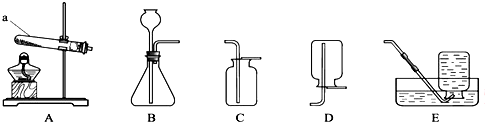



 ,B中的官能团名称是醛基、羟基.
,B中的官能团名称是醛基、羟基. .
. .
.


 .
. .
. ,反应类型酯化反应.
,反应类型酯化反应. )
) .
.