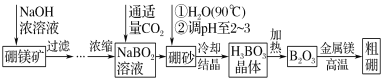
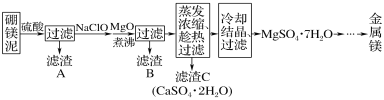
��Ŀ����
����Ŀ���Ȼ���ͭ(CuCl)����ʰ�ɫ������ֽ⣬¶���ڳ�ʪ�������ױ�������ij�о�С������������ַ�����ʵ�����Ʊ��Ȼ���ͭ��
����һ��ͭ�ۻ�ԭCuSO4��Һ
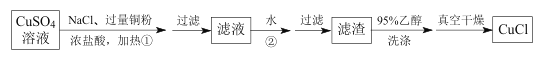
��֪��CuCl������ˮ���Ҵ�����ˮ��Һ�д���ƽ�⣺CuCl(��ɫ)+2Cl-![]() [CuCl3] 2-(��ɫ��Һ)��
[CuCl3] 2-(��ɫ��Һ)��
(1)������з�����Ӧ�����ӷ���ʽΪ________________��
(2)������У��������ˮ��������_____________ ��
(3)��ͼ��������95%�Ҵ�ϴ�Ӻ���ո�����Ϊ�˷�ֹ________________ ��
�����������Ȼ��������м���CuCl22H2O�����Ʊ��������̺�ʵ��װ��(�г�������)���£�
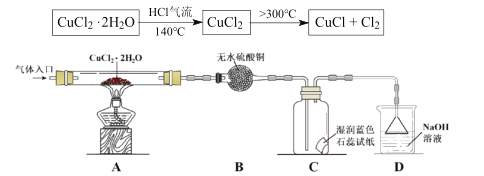
��ش��������⣺
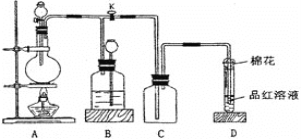
(4)ʵ��������Ⱥ�˳���� a��_____��______��_______��e (������ı��)
a�����װ�õ������Ժ����ҩƷ b����ȼ�ƾ��ƣ�����
c���ڡ�������ڡ���ͨ�����HCl d��Ϩ��ƾ��ƣ���ȴ
e��ֹͣͨ��HCl��Ȼ��ͨ��N2
(5)��ʵ������У��۲쵽B�������ɰ�ɫ��Ϊ��ɫ��C����ֽ����ɫ�仯��______��
(6)��Ӧ������ȡ��CuCl��Ʒ����ʵ�飬�������к���������CuCl2���ʣ����������CuCl2���ʵ�ԭ�� ________________________��
(7)ȷ��ȡ0. 2500 g�Ȼ���ͭ��Ʒ����һ������0.5 mol/L FeCl3��Һ�У�����Ʒ��ȫ�ܽ��ˮ20 mL����0. 1000 mol/L��Ce(SO4)2��Һ�ζ����յ㣬����24. 60 mLCe(SO4)2��Һ���йػ�ѧ��ӦΪFe3++CuCl=Fe2++Cu2++Cl-��Ce4++Fe2+=Fe3++Ce3+������������Ʒ��CuCl������������_____________ %(�𰸱���4λ��Ч����)��
���𰸡�Cu+Cu2++6Cl-=2[CuCl3]2- ϡ�ʹٽ�ƽ��CuCl(��ɫ)+2Cl-![]() [CuCl3]2-(��ɫ��Һ)�����ƶ�������CuCl CuCl�ڳ�ʪ�����б����� c b d �ȱ�����ɫ ����ʱ�䲻����¶�ƫ�� 97.92
[CuCl3]2-(��ɫ��Һ)�����ƶ�������CuCl CuCl�ڳ�ʪ�����б����� c b d �ȱ�����ɫ ����ʱ�䲻����¶�ƫ�� 97.92
��������
����һ��CuSO4��Cu��NaCl��Ũ������������¼��ȣ�������Ӧ��Cu+Cu2++6Cl-=2[CuCl3]2-�����˳�ȥ������ͭ�ۣ�Ȼ���ˮϡ����Һ����ѧƽ��CuCl(��ɫ)+2Cl-![]() [CuCl3]2-(��ɫ��Һ)�����ƶ����õ�CuCl��������95%���Ҵ�ϴ�Ӻ�Ϊ��ֹ��ʪ������CuCl������������ջ����и���õ�����CuCl��
[CuCl3]2-(��ɫ��Һ)�����ƶ����õ�CuCl��������95%���Ҵ�ϴ�Ӻ�Ϊ��ֹ��ʪ������CuCl������������ջ����и���õ�����CuCl��
��������CuCl2�ǻӷ���ǿ�����ɵ������Σ���CuCl2��2H2O������HCl�����м�����ˮ�õ���ˮCuCl2��Ȼ���ڸ���300�����¶��¼��ȣ������ֽⷴӦ����CuCl��Cl2��
(1)�������CuSO4��Cu����������ԭ��Ӧ��������Cu+����Һ��Cl-����γ�[CuCl3]2-��������Ӧ�����ӷ���ʽΪ��Cu+Cu2++6Cl-=2[CuCl3]2-��
(2)������֪������CuCl������ˮ���Ҵ�����ˮ��Һ�д���ƽ�⣺CuCl(��ɫ)+2Cl-![]() [CuCl3] 2-(��ɫ��Һ)���ڲ��������Ӧ�����Һ�м��������ˮ����Һ��Cl-��[CuCl3] 2-Ũ�ȶ���С������Ӧ���ʼ�С�ı��������淴Ӧ���ʼ�С�ı��������Ի�ѧƽ�������ƶ����Ӷ�����CuCl������
[CuCl3] 2-(��ɫ��Һ)���ڲ��������Ӧ�����Һ�м��������ˮ����Һ��Cl-��[CuCl3] 2-Ũ�ȶ���С������Ӧ���ʼ�С�ı��������淴Ӧ���ʼ�С�ı��������Ի�ѧƽ�������ƶ����Ӷ�����CuCl������
(3)�Ҵ��ӷ�����95%�Ҵ�ϴ�ӿ���ȥ��CuCl�ϵ�ˮ�֣���ո���Ҳ���Ա���CuCl�ڳ�ʪ�����б�������
(4)CuCl22H2O����Ҫ��HCl�����м��ȣ�����ʵ��ǰҪ�ȼ��װ�õ������ԣ������������������ͨ�����HCl��Ȼ���ȼ�ƾ��ƣ����ȣ���������ȫ�ֽ��IJ�����Ϩ��ƾ��ƣ���ȴ��Ϊ�˽�װ���в�����HCl�ų�����ֹ��Ⱦ������Ҫֹͣͨ��HCl��Ȼ��ͨ��N2����ʵ�������ŵ��Ⱥ�˳���� a��c��b��d��e��
(5)��ˮ����ͭ�ǰ�ɫ���壬��������ˮʱ�γ�CuSO4��5H2O�������Ϊ��ɫ��HCl������ˮ��Ϊ���ᣬ��Һ�����ԣ�ʹʪ�����ɫʯ����ֽ��Ϊ��ɫ����CuCl2�ٽ�һ�����ȷֽ�ʱ������Cl2��Cl2��H2O��Ӧ����HCl��HClO��HCʹʪ�����ɫʯ����ֽ��Ϊ��ɫ��HClO����ǿ�����ԣ���ʹ��Ϊ��ɫ��ʯ����ֽ��ɫ��Ϊ��ɫ��
(6)��Ӧ������ȡ��CuCl��Ʒ����ʵ�飬�������к���������CuCl2���ʣ�����CuCl2���ʵ�ԭ������Ǽ���ʱ�䲻�������¶�ƫ�ͣ�ʹCuCl2δ��ȫ�ֽ⣻
(7)���ݷ�Ӧ����ʽFe3++CuCl=Fe2++Cu2++Cl-��Ce4++Fe2+=Fe3++Ce3+�ɵù�ϵʽ��CuCl��Ce4+��24. 60 mL 0. 1000 mol/L��Ce(SO4)2��Һ�к�������Ce(SO4)2�����ʵ���n[Ce(SO4)2]=0. 1000 mol/L��0.02460 L=2.46��10-3 mol������ݹ�ϵʽ��֪n(CuCl)=n(Ce4+)=2.46��10-3 mol��m(CuCl)=2.46��10-3 mol��99.5 g/mol=0.24478 g�����Ը���Ʒ��CuCl������������![]() ��100%=97.92%��
��100%=97.92%��

 ��ʦ����ָ���ο�ʱϵ�д�
��ʦ����ָ���ο�ʱϵ�д�