题目内容
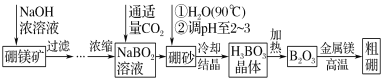
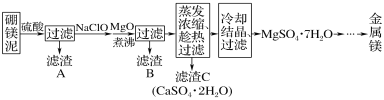
【题目】硼单质在高温时是良好的导体,也是用途广泛的化工原料。镁单质可用于制造轻金属合金、球墨铸铁等。硼镁矿的主要成分为Mg2B2O5·H2O,可以制取单质硼和镁。制取工艺流程如图所示,已知硼砂的化学式为Na2B4O7·10H2O,硼镁泥是硼镁矿制硼砂过程中产生的废渣,其主要成分是MgCO3,还含有CaO、Al2O3、Fe2O3、FeO、MnO、SiO2等杂质。按要求回答问题:
(1)化合物Mg2B2O5·H2O中B的化合价为_____。
(2)将硼砂溶于热水后,常用稀硫酸调pH至2~3制取H3BO3,该反应的离子方程式为____。
(3)写出加NaClO的过程中发生反应的离子方程式:________;________。
(4)将硼镁泥中加入的硫酸改为盐酸是否可行?___。(填“是”或“否”),理由是____。
【答案】+3 B4O72-+2H++5H2O=4H3BO3 Mn2++ClO-+H2O=MnO2↓+Cl-+2H+ 2Fe2++ClO-+2H+=2Fe3++Cl-+H2O 否 改为盐酸后,硼镁泥中的CaO转化为CaCl2,CaCl2易溶于水,无法除去杂质钙离子
【解析】
(1)Mg2B2O5·H2O中Mg元素的化合价为+2价,H元素的化合价为+1价,O元素的化合价为-2价,根据化合物中各元素化合价代数和为零可得到Mg2B2O5·H2O中硼元素的化合价为+3,故答案为:+3。
(2)硼砂在酸溶液中生成一元弱酸H3BO3的离子方程式为B4O72-+2H++5H2O=4H3BO3,故答案为:B4O72-+2H++5H2O=4H3BO3。
(3)由题图2及硼镁泥的成分可,往硼镁泥中加硫酸得到的滤渣A的主要成分为SiO2,向滤液中加次氯酸钠可以将滤液中的Fe2+和Mn2+氧化,所以加入NaClO的过程中发生反应的离子方程式为:Mn2++ClO-+H2O=MnO2↓+Cl-+2H+、2Fe2++ClO-+2H+=2Fe3++Cl-+H2O,故答案为:Mn2++ClO-+H2O=MnO2↓+Cl-+2H+、2Fe2++ClO-+2H+=2Fe3++Cl-+H2O。
(4)CaSO4微溶于水,CaCl2易溶于水,改为盐酸后,硼镁泥中的CaO转化为CaCl2,CaCl2易溶于水,无法除去杂质钙离子,故答案为:否;改为盐酸后,硼镁泥中的CaO转化为CaCl2,CaCl2易溶于水,无法除去杂质钙离子。