题目内容
13.阿伏加德罗常数约为6.02×1023mol-1,下列叙述正确的是( )| A. | 58.5 g的氯化钠固体中含有NA个氯化钠分子 | |
| B. | 0.1 L 3 mo1•L-1的NH4NO3溶液中含有的NH4+数目为0.3×6.02×1023 | |
| C. | 5.6 g铁粉与硝酸反应失去的电子数一定为0.3×6.02×1023 | |
| D. | 4.5 g SiO2晶体中含有的硅氧键数目为0.3×6.02×1023 |
分析 A、氯化钠为离子晶体;
B、NH4+是弱碱阳离子,在溶液中水解;
C、硝酸具有强氧化性,5.6g铁粉与硝酸反应生成硝酸铁或硝酸亚铁或硝酸铁、硝酸亚铁混合物;
D、依据n=$\frac{m}{M}$计算物质的量,结合1mol二氧化硅晶体中含硅氧键计算得到.
解答 解:A、氯化钠为离子晶体,故氯化钠固体中无氯化钠分子,故A错误;
B、NH4+是弱碱阳离子,在溶液中水解,故溶液中的NH4+数目小于0.3×6.02×1023,故B错误;
C、铁粉与硝酸反应生成硝酸铁或硝酸亚铁或硝酸铁、硝酸亚铁混合,5.6g铁粉的物质的量为0.1mol,5.6g铁粉完全反应失去的电子的物质的量为0.2mol或0.3mol或介于0.2mol~0.3mol之间,故C错误;
D、4.5gSiO2晶体物质的量=$\frac{4.5g}{60g/mol}$=0.75mol,含有的硅氧键数目为0.75mol×4×NA=0.3×6.02×1023 ,故D正确;
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
3.卤族元素随核电荷数的增加,下列叙述正确的是( )
| A. | 单质的颜色逐渐加深 | B. | 气态氢化物的稳定性逐渐增强 | ||
| C. | 单质的熔点逐渐升高 | D. | 单质的氧化性逐渐增强 |
1.实验室中需要配制2mol/L的NaCl溶液950mL,配制时应选用的容量瓶的规格和称取的NaCl的质量分别是
( )
( )
| A. | 950 mL 111.2 g | B. | 500 mL 117.0 g | ||
| C. | 1000 mL 117.0 g | D. | 1000 mL 111.2 g |
8.某地污水中含有Zn2+、Hg2+、Fe3+和Cu2+4种阳离子.甲、乙、丙3位同学设计的从该污水中回收金属铜的方案如下.
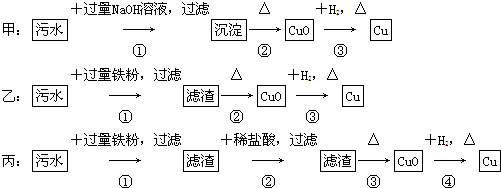
下列判断正确的是( )

下列判断正确的是( )
| A. | 三种实验方案中都能制得纯净的铜 | |
| B. | 乙方案中加过量铁粉可以将4种阳离子全部还原 | |
| C. | 甲方案中的反应涉及置换、分解、化合、复分解4种反应类型 | |
| D. | 丙方案会产生环境污染 |
2.下列物质所形成的晶体中阴阳离子的个数比为1:1的是( )
| A. | Na2O2 | B. | NaHSO4 | C. | HCl | D. | H2O |
3.下列实验装置(固定装置略去)和操作正确的是( )
| A. | 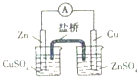 构成铜锌原电池 | B. | 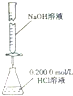 酸碱中和滴定 | C. | 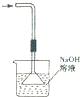 吸收HCl尾气 | D. | 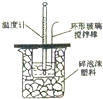 中和热的测定 |