题目内容
【题目】在一个固定容积的密闭容器中,保持一定温度进行如下反应:H2(g)+Br2(g)![]() 2HBr(g),已知加入1 mol H2和2 mol Br2达到平衡后,生成x mol HBr,在相同条件下若起始时加入的H2、Br2、HBr分别为a、b、c(均不为0)且保持平衡时,各组分含量都不变,以下推断正确的是
2HBr(g),已知加入1 mol H2和2 mol Br2达到平衡后,生成x mol HBr,在相同条件下若起始时加入的H2、Br2、HBr分别为a、b、c(均不为0)且保持平衡时,各组分含量都不变,以下推断正确的是
①a、b、c应满足的关系是4a+c=2b
②平衡时HBr为ax mol
③a、b、c应满足的关系是a+b=c
④平衡时HBr为![]() x mol
x mol
A. ① B. ①② C. ①④ D. ②③
【答案】C
【解析】
在容器中充入1molH2和2molBr2达到平衡后生成xmolHBr。在相同条件下,若起始时加入H2、Br2、HBr分别为amol、bmol、cmol(均不为0),达到平衡时,各组分百分含量和前一平衡相同,则建立的是等效平衡;由于该反应是气体体积不变的反应,将所有量按照反应方程式转化成氢气和溴,只要满足n(H2):n(Br2)=1mol:2mol=1:2即可。①根据极限转化的思想,将cmol的HBr极限转化为反应物,要实现等效平衡的建立,则相当于的投料符合:氢气:a+![]() =1,溴单质:b+
=1,溴单质:b+![]() =2,整理得到:4a+c=2b,故①正确;②反应两边气体的体积不变,在容器中充入1molH2和2molBr2达到平衡后气体的物质的量还是3mol,则溴化氢的百分含量为
=2,整理得到:4a+c=2b,故①正确;②反应两边气体的体积不变,在容器中充入1molH2和2molBr2达到平衡后气体的物质的量还是3mol,则溴化氢的百分含量为![]() ,加入H2、Br2、HBr分别为amol、bmol、cmol(均不为0),达到平衡时两个平衡中溴化氢的百分含量相等,设达到平衡时HBr物质的量为m,则
,加入H2、Br2、HBr分别为amol、bmol、cmol(均不为0),达到平衡时两个平衡中溴化氢的百分含量相等,设达到平衡时HBr物质的量为m,则![]() =
= ![]() ,所以m=
,所以m=![]() xmol,即达到平衡时HBr物质的量为
xmol,即达到平衡时HBr物质的量为![]() xmol,故②错误,④正确;③根据①可知,4a+c=2b,所以a+b不一定等于c,故③错误;根据分析可知,正确的为①④,故选C。
xmol,故②错误,④正确;③根据①可知,4a+c=2b,所以a+b不一定等于c,故③错误;根据分析可知,正确的为①④,故选C。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】有七种元素,其中A、X、Y、D、E为短周期主族元素,Z、G为第四周期元素,它们的原子序数依次增大。请回答问题。
A | 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
X | 元素原子的核外 |
Y | 原子的第一至第四电离能分别是: |
D | 原子核外所有 |
E | 元素的主族序数与周期数的差为4 |
Z | 是前四周期中电负性最小的元素 |
G | 在周期表的第七列 |
(1)已知![]() 为离子化合物,写出其电子式_______________。
为离子化合物,写出其电子式_______________。
(2)X基态原子中能量最高的电子,其电子云在空间有______个方向,原子轨道呈_____形;![]() 的空间构型为__________。
的空间构型为__________。
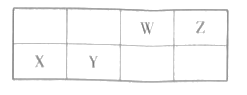
(3)某同学根据上述信息,推断Y基态原子的核外电子排布为:
![]()
该同学所画的电子排布图违背了________________________。
(4)G位于元素周期表的_________区,原子结构示意图为____________________。
(5)![]() 中心原子的杂化方式为_________,其空间构型为____________________。
中心原子的杂化方式为_________,其空间构型为____________________。
(6)Z元素的基态原子价电子排布式为_______________________。