题目内容
【题目】某同学在实验室进行铁盐与亚铁盐相互转化的实验:
实验I:将Fe3+转化为Fe2+
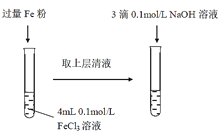
(1)常温下,FeCl3溶液显酸性,用离子方程式表示其显酸性的原因___。
(2)Fe3+与Fe粉发生反应的离子方程式为___。
(3)滴加NaOH溶液观察到的现象为___。
实验II:将Fe2+转化为Fe3+
实验方案 | 现象 |
向3mL0.1mol/LFeSO4溶液中加入1mL8mol/L稀硝酸 | 溶液变为棕色,放置一段时间后,棕色消失,溶液变为黄色 |
探究上述现象出现的原因:
查阅资料:Fe2++NO![]() Fe(NO)2+(棕色)
Fe(NO)2+(棕色)
(4)用离子方程式解释NO产生的原因___。
(5)从化学反应限度的角度对体系中存在的反应进行反应I:Fe2+与HNO3反应;反应II:Fe2+与NO反应
①乙认为反应I是一个不可逆反应,并通过实验证明其猜测正确,乙设计的实验方案是___。
②查阅资料反应I的速率比反应II慢,请用化学平衡移动原理解释溶液由棕色变为黄色的原因___。
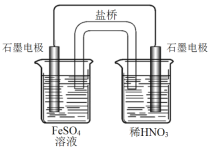
(6)丙认为若生成的NO与Fe2+不接触,溶液就不会出现棕色,请画出实验装置图,实现Fe2+![]() Fe3+的转化,同时避免出现此异常现象。___
Fe3+的转化,同时避免出现此异常现象。___
【答案】Fe3++3H2O![]() Fe(OH)3+3H+ Fe3++2Fe=3Fe2+ 有灰白色沉淀产生,迅速转变为灰绿色,最终转变为红褐色 3Fe2++4H+ +NO3-=3Fe3++NO↑+2H2O 取反应后的黄色溶液于试管中,向其中加入几滴K3Fe(CN)6溶液,无明显变化,说明反应Ⅰ是不可逆反应 Fe2+被HNO3氧化,导致Fe2+浓度降低,使平衡Fe2++NO
Fe(OH)3+3H+ Fe3++2Fe=3Fe2+ 有灰白色沉淀产生,迅速转变为灰绿色,最终转变为红褐色 3Fe2++4H+ +NO3-=3Fe3++NO↑+2H2O 取反应后的黄色溶液于试管中,向其中加入几滴K3Fe(CN)6溶液,无明显变化,说明反应Ⅰ是不可逆反应 Fe2+被HNO3氧化,导致Fe2+浓度降低,使平衡Fe2++NO![]() Fe(NO)2+逆向移动,最终Fe(NO)2+完全转化为Fe3+,溶液由棕色变为黄色
Fe(NO)2+逆向移动,最终Fe(NO)2+完全转化为Fe3+,溶液由棕色变为黄色 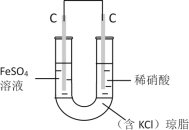
【解析】
常温下,Fe3+水解使溶液呈酸性,Fe3++3H2O![]() Fe(OH)3+3H+;
Fe(OH)3+3H+;
Fe3+与Fe粉发生反应的离子方程式为Fe3++2Fe=3Fe2+;
滴加NaOH溶液观察到的现象为有灰白色沉淀产生,迅速转变为灰绿色,最终转变为红褐色;
由于发生氧化还原反应,产生NO,方程式为3Fe2++4H+ +NO3-=3Fe3++NO↑+2H2O;
①取反应后的黄色溶液于试管中,向其中加入几滴K3Fe(CN)6溶液,无明显变化,说明反应Ⅰ是不可逆反应;
②Fe2+被HNO3氧化,导致Fe2+浓度降低,使平衡Fe2++NO![]() Fe(NO)2+逆向移动,最终Fe(NO)2+完全转化为Fe3+,溶液由棕色变为黄色;
Fe(NO)2+逆向移动,最终Fe(NO)2+完全转化为Fe3+,溶液由棕色变为黄色;
丙认为若生成的NO与Fe2+不接触,溶液就不会出现棕色,可设计为双液原电池,实现Fe2+![]() Fe3+的转化,
Fe3+的转化, 。
。

 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案【题目】相同温度、相同容积的四个密闭容器中进行同样的可逆反应:2X(g)+Y(g)![]() 3W(g)+2Z(g) △H=﹣Q KJ/mol,起始时充入气体的物质的量及平衡时体系能量变化数据如表,下列说法正确的是( )
3W(g)+2Z(g) △H=﹣Q KJ/mol,起始时充入气体的物质的量及平衡时体系能量变化数据如表,下列说法正确的是( )
X | Y | W | Z | 反应体系能量变化 | |
甲 | 2mol | 1mol | 放出a kJ/mol | ||
乙 | 1mol | 1mol | 放出b kJ/mol | ||
丙 | 2mol | 2mol | 放出c kJ/mol | ||
丁 | 3mol | 2mol | 吸收d kJ/mol |
A.X的转化率为:甲<乙<丙
B.c+d<Q
C.平衡时,甲容器中的反应速率比丁容器中的慢
D.平衡时丙容器中Z的物质的量浓度最大
【题目】人体血液中存在的平衡:H2CO3 ![]() HCO3-,使血液pH保持在7.35 ~ 7.45之间,否则就会发生酸中毒或碱中毒。已知pH随
HCO3-,使血液pH保持在7.35 ~ 7.45之间,否则就会发生酸中毒或碱中毒。已知pH随 变化关系如表所示,则下列说法中错误的是
变化关系如表所示,则下列说法中错误的是
| 1.0 | 17.8 | 20.0 | 22.4 |
pH | 6.10 | 7.35 | 7.40 | 7.45 |
A.pH=7的血液中,c(HCO3-)>c(H2CO3)
B.正常体温下人体发生碱中毒时,c(H+)c(OH-)变大
C.人体发生酸中毒时,可静脉滴注一定浓度的NaHCO3溶液解毒
D. =20.0时,H2CO3的电离程度小于HCO3-的水解程度
=20.0时,H2CO3的电离程度小于HCO3-的水解程度