��Ŀ����
����Ŀ����ͬ�¶ȡ���ͬ�ݻ����ĸ��ܱ������н���ͬ���Ŀ��淴Ӧ��2X(g)+Y(g)![]() 3W(g)+2Z(g) ��H=��Q KJ/mol����ʼʱ������������ʵ�����ƽ��ʱ��ϵ�����仯�������������˵����ȷ���ǣ�������
3W(g)+2Z(g) ��H=��Q KJ/mol����ʼʱ������������ʵ�����ƽ��ʱ��ϵ�����仯�������������˵����ȷ���ǣ�������
X | Y | W | Z | ��Ӧ��ϵ�����仯 | |
�� | 2mol | 1mol | �ų�a kJ/mol | ||
�� | 1mol | 1mol | �ų�b kJ/mol | ||
�� | 2mol | 2mol | �ų�c kJ/mol | ||
�� | 3mol | 2mol | ����d kJ/mol |
A.X��ת����Ϊ���ף��ң���
B.c+d��Q
C.ƽ��ʱ���������еķ�Ӧ���ʱȶ������е���
D.ƽ��ʱ��������Z�����ʵ���Ũ�����
���𰸡�D
��������
A���������ʵ������ҵ�2�������ʵ�������ѹǿ����ת���ʼ�С����ת������>����������ȣ�����������X�����ʵ�������X��ת���ʼ�С����ת���ʼף��ң��������ʵ����൱���ڼĻ�����������Y����X��ת�������ף���������X��ת����Ϊ����>��>�ף���A����
B�������ڵ�Чƽ�⣬���߷�Ӧ�����෴�����ߵ�ת����֮��Ϊ100%���������֮��ΪQ�����ļ���Y�������ڼף�����������еij̶ȴ����Ա��ų����������ڼף����������֮�ʹ���Q����c+d>Q����B����
C�����ݷ�Ӧ2X(g)+Y(g)![]() 3W(g)+2Z(g)��֪���ں��º��������£���ʼʱ2molX��1molY�൱�ڼ���3molW��2molZ����������ƽ�⻥Ϊ��Чƽ�⣬��ƽ��ʱ�����Ũ����ȣ�����ƽ��ʱ�ס��������еķ�Ӧ������ȣ���C����
3W(g)+2Z(g)��֪���ں��º��������£���ʼʱ2molX��1molY�൱�ڼ���3molW��2molZ����������ƽ�⻥Ϊ��Чƽ�⣬��ƽ��ʱ�����Ũ����ȣ�����ƽ��ʱ�ס��������еķ�Ӧ������ȣ���C����
D�����п��Կ����ȼ���2molX��1molY��ƽ����ּ���1molY������Ӧ���Ũ��ƽ�������ƶ��������������Ũ����������Z�����ʵ���Ũ�����D��ȷ��
�ʴ�Ϊ��D��

����Ŀ��25 ��ʱ�й����ʵ���ɫ���ܶȻ���Ksp�����±���
���� | AgCl | AgBr | AgI | Ag2S |
��ɫ | �� | ���� | �� | �� |
Ksp | 1.8��10��10 | 7.7��10��13 | 1.5��10��16 | 1.8��10��50 |
���������в���ȷ���ǣ�������
A.��AgCl�İ�ɫ����Һ�м���0.1 mol/L KI��Һ���л�ɫ��������
B.25 ��ʱ�����ñ��е��ܶȻ���Ksp�������Լ���AgCl��AgBr��AgI��Ag2S����ˮ��Һ��Ag����Ũ��
C.25 �棬AgCl����ֱ��ڵ����ʵ���Ũ��NaCl��CaCl2��Һ���ܽ�ﵽƽ�⣬����Һ�У�c��Ag+�����ܶȻ�����ͬ
D.��5 mL 1.8��10��6 mol/L NaCl��Һ�У�����1�Σ�20��ԼΪ1 mL��1��10��3 mol/L AgNO3��Һ�����ܲ�����ɫ����
����Ŀ��ijͬѧ��ʵ���ҽ����������������ת����ʵ�飺
ʵ��I����Fe3+ת��ΪFe2+
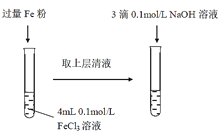
��1�������£�FeCl3��Һ�����ԣ������ӷ���ʽ��ʾ�������Ե�ԭ��___��
��2��Fe3+��Fe�۷�����Ӧ�����ӷ���ʽΪ___��
��3���μ�NaOH��Һ�۲쵽������Ϊ___��
ʵ��II����Fe2+ת��ΪFe3+
ʵ�鷽�� | ���� |
��3mL0.1mol/LFeSO4��Һ�м���1mL8mol/Lϡ���� | ��Һ��Ϊ��ɫ������һ��ʱ�����ɫ��ʧ����Һ��Ϊ��ɫ |
̽������������ֵ�ԭ��
�������ϣ�Fe2++NO![]() Fe(NO)2+����ɫ��
Fe(NO)2+����ɫ��
��4�������ӷ���ʽ����NO������ԭ��___��
��5���ӻ�ѧ��Ӧ�ȵĽǶȶ���ϵ�д��ڵķ�Ӧ���з�ӦI��Fe2+��HNO3��Ӧ����ӦII��Fe2+��NO��Ӧ
������Ϊ��ӦI��һ�������淴Ӧ����ͨ��ʵ��֤����²���ȷ������Ƶ�ʵ�鷽����___��
�ڲ������Ϸ�ӦI�����ʱȷ�ӦII�������û�ѧƽ���ƶ�ԭ��������Һ����ɫ��Ϊ��ɫ��ԭ��___��
��6������Ϊ�����ɵ�NO��Fe2+���Ӵ�����Һ�Ͳ��������ɫ���뻭��ʵ��װ��ͼ��ʵ��Fe2+![]() Fe3+��ת����ͬʱ������ִ��쳣����___
Fe3+��ת����ͬʱ������ִ��쳣����___
