题目内容
5. 已知砷(As)元素的原子结构示意图为
已知砷(As)元素的原子结构示意图为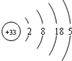
(1)砷在元素周期表中位于第四周期,最高正化合价为+5.
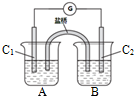
(2)已知可逆反应AsO43-+2I-+2H+?AsO33-+I2+H2O.如图所示,若A中盛KI和I2溶液,B中盛Na3AsO4和Na3AsO3溶液,C1、C2为两根碳棒.当向B中滴加浓盐酸时,发现G中的指针发生偏转;改向B中滴加40%的NaOH溶液时,G中的指针则向反方向偏转.
①加盐酸时,上述平衡向右(正反应)移动,C1是负极(填“正”或“负”);
②写出加NaOH溶液时,C2上发生的电极反应式AsO33-+I2+2OH-?AsO43-+2I-+H2O.
(3)As2O3俗名砒霜,是一种剧毒物质.法医检验砒霜中毒的方法是:向试样中加入锌粉和盐酸,如果有砒霜,将生成无色气体AsH3,将气体导入热玻璃管会分解成亮黑色的“砷镜”,这就是著名的“马氏验砷法”.请写出上述生成AsH3的化学方程式As2O3+6Zn+12HCl=2AsH3↑+6ZnCl2+3H2O.
分析 (1)电子层等于周期序数,最外层电子数等于最高正化合价;
(2)①加盐酸时,可逆反应AsO43-+2I-+2H+?AsO33-+I2+H2O,氢离子的浓度变大,平衡正向移动,A中碘离子发生氧化反应为负极,所以C1为负极;
②该电极反应式为AsO33-+I2+2OH-?AsO43-+2I-+H2O;
(3)根据题目信息砒霜、锌粉和盐酸为反应物,生成物之一为AsH3,根据质量守恒定律可写出反应的化学方程式.
解答 解:(1)电子层等于周期序数,4个电子层,所以周期数为:四,最外层有5个电子,所以最高正价为+5,故答案为:四;+5;
(2)①加盐酸时,可逆反应AsO43-+2I-+2H+?AsO33-+I2+H2O,氢离子的浓度变大,平衡正向移动,A中碘离子发生氧化反应为负极,所以C1为负极,
故答案为:右(正反应); 负;
②加NaOH溶液时平衡逆向移动,该过程中C2棒为负极失电子发生氧化反应,电极反应为AsO33-+2OH--2e-=AsO43-+H2O,
故答案为:AsO33-+2OH--2e-=AsO43-+H2O;
(3)根据题目信息砒霜、锌粉和盐酸为反应物,生成物之一为AsH3,根据质量守恒定律可写出反应的化学方程式As2O3+12HCl+6Zn=6ZnCl2+2AsH3↑+3H2O,
故答案为:As2O3+6Zn+12HCl=2AsH3↑+6ZnCl2+3H2O.
点评 本题考查原子结构确定元素在周期表中的位置,结合电化学考查平衡移动,根据题意书写化学方程式,学生要在读懂题目条件的情况下解题,考查学生筛选信息的能力,比较容易.

练习册系列答案
相关题目
16.下列实验能达到目的是( )
| A. |  测定乙醇结构式 | B. | 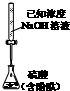 测定硫酸浓度 | ||
| C. | 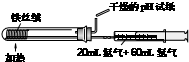 合成并检验氨 | D. | 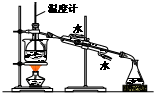 分离并回收硝基苯中的苯 |
13.化学与社会、生活密切相关.如表中的事实和解释均正确的是( )
| 选项 | 事实 | 解释 |
| A | 用热的纯碱溶液洗去油污 | Na2CO3可作为油脂分解的催化剂 |
| B | 铝罐车可用于运输稀硝酸 | 铝表面形成致密氧化膜具有保护作用 |
| C | 甘油作为化妆品中的保湿剂 | 甘油易与水形成氢键 |
| D | 氢氟酸刻蚀水晶工艺品 | HF具有强酸性 |
| A. | A | B. | B | C. | C | D. | D |
20.氮及其化合物在工农业生产、生活中有重要作用.请按要求回答下列相关问题:
(1)食品添加剂铵明矾NH4Al(SO4)2•12H2O高温可分解,下列关于其分解产物的预测不合理 的是C.
A.NH3、N2、SO2、H2O B.NH3、SO3、H2O
C.NH3、SO2、H2O D.NH3、N2、SO3、SO2、H2O
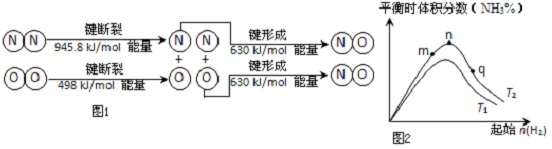
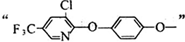
(2)汽车发动机工作时也会引发N2和O2反应产生大气污染物NO,其能量变化示意图如图1则该反应的热化学方程式为N2(g)+O2(g)=2NO(g)△H=+183.8kJ/mol.
(3)工业合成氨的反应:N2(g)+3H2(g)?2NH3(g)△H<0,分别在T1、T2温度下,改变起始氢气物质的量,测得平衡时氨的体积分数如图2所示:
①比较在m、n、q三点所处的平衡状态中,反应物N2的转化率最高的是P点.
②T2条件下,在2L的密闭容器中,充入x mol N2和 y mol H2时,3min达平衡,此时反应物的转化率均为a,写出下列仅含a、x的表达式(不必化简):v(N2)=$\frac{xa}{6}$mol•L-1•min-1;该反应的平衡常数的值K=$\frac{16(xa){\;}^{2}}{(x-xa)(3x-3xa){\;}^{3}}$.
③图象中T2低于T1(填“高于”、“低于”、“等于”或“无法确定”).
④科学家采用高质子导电性的SCY陶瓷(能传递H+ )实现氨的电化学合成,这提高了氮气和氢气的转化率.写出电化学合成过程中发生还原反应的电极方程式:N2+6H++6e-=2NH3.
(4)将质量相等的四份铁粉和铜粉的均匀混合物,分别加入同浓度稀硝酸充分反应,(假设硝酸的还原产物只有NO)实验数据如下表:
下列有关分析推断正确的是AC.
A.硝酸起始浓度为4mol/L B.①中溶解了5.6g Fe
C.③中n(Cu2+)=0.15mol D.④中V=6.72L
(1)食品添加剂铵明矾NH4Al(SO4)2•12H2O高温可分解,下列关于其分解产物的预测不合理 的是C.
A.NH3、N2、SO2、H2O B.NH3、SO3、H2O
C.NH3、SO2、H2O D.NH3、N2、SO3、SO2、H2O
(2)汽车发动机工作时也会引发N2和O2反应产生大气污染物NO,其能量变化示意图如图1则该反应的热化学方程式为N2(g)+O2(g)=2NO(g)△H=+183.8kJ/mol.
(3)工业合成氨的反应:N2(g)+3H2(g)?2NH3(g)△H<0,分别在T1、T2温度下,改变起始氢气物质的量,测得平衡时氨的体积分数如图2所示:
①比较在m、n、q三点所处的平衡状态中,反应物N2的转化率最高的是P点.
②T2条件下,在2L的密闭容器中,充入x mol N2和 y mol H2时,3min达平衡,此时反应物的转化率均为a,写出下列仅含a、x的表达式(不必化简):v(N2)=$\frac{xa}{6}$mol•L-1•min-1;该反应的平衡常数的值K=$\frac{16(xa){\;}^{2}}{(x-xa)(3x-3xa){\;}^{3}}$.
③图象中T2低于T1(填“高于”、“低于”、“等于”或“无法确定”).
④科学家采用高质子导电性的SCY陶瓷(能传递H+ )实现氨的电化学合成,这提高了氮气和氢气的转化率.写出电化学合成过程中发生还原反应的电极方程式:N2+6H++6e-=2NH3.
(4)将质量相等的四份铁粉和铜粉的均匀混合物,分别加入同浓度稀硝酸充分反应,(假设硝酸的还原产物只有NO)实验数据如下表:
| 编 号 | ① | ② | ③ | ④ |
| 稀硝酸体积/mL | 100mL | 200mL | 300mL | 400mL |
| 剩余金属/g | 18.0g | 9.6g | 0 | 0 |
| NO体积/L(标准状况下) | 2.24L | 4.48L | 6.72L | V |
A.硝酸起始浓度为4mol/L B.①中溶解了5.6g Fe
C.③中n(Cu2+)=0.15mol D.④中V=6.72L

10.(多项选择题)下列说法中正确的是( )
| A. | SO3、NO3-、BF3都是平面三角型 | B. | P4、CS2、PH3都是非极性分子 | ||
| C. | 金刚石、石墨、SiC都是原子晶体 | D. | 第一电离能:N>O>C |
15.下列物质属于油脂的是( )
| A. | 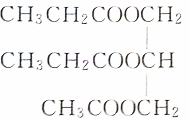 | B. | 润滑油 | ||
| C. | 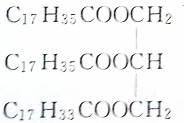 | D. | 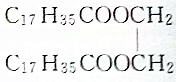 |
 ;
;
 .
.