题目内容
17.天然气是一种重要的清洁能源和化工原料,其主要成分为甲烷.(1)已知:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H1
CO(g)+H2O(g)═CO2(g)+H2(g)△H2
2CO(g)+O2(g)═2CO2(g)△H3
则CO2(g)+CH4(g)═2CO(g)+2H2(g)的△H=△H1+2△H2-2△H3.
(2)天然气中的少量H2S杂质常用氨水吸收,产物为NH4HS.一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式2NH4HS+O2=2NH3•H2O+2S↓.
(3)天然气的一个重要用途是制取H2,其原理为:CO2(g)+CH4(g)?2CO(g)+2H2(g).
①该反应的平衡常数表达式为K=$\frac{c{\;}^{2}(CO)•c{\;}^{2}(H{\;}_{2})}{c(CO{\;}_{2})•c(CH{\;}_{4})}$.
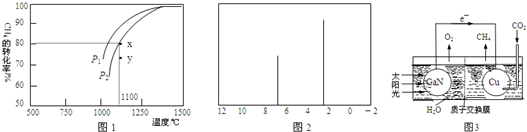
②在密闭容器中通入物质的量浓度均为0.1mol•L-1的CH4与CO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如图l所示.则压强P1小于P2 (填“大于”或“小于”);压强为P2时,在Y点:v(正)大于v(逆)(填“大于“、“小于”或“等于“).
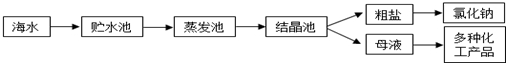
(4)天然气也可重整生产化工原料,最近科学家们利用天然气无氧催化重整获得芳香烃X.由质谱分析得X的相对分子质量为l06,其核磁共振氢谱如图2所示,则X的结构简式为
 .
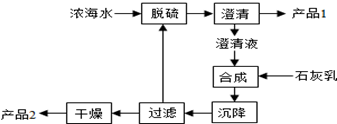
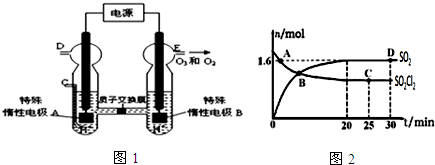
.(5)科学家用氮化镓材料与铜组装如图3所示人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4.
①写出铜电极表面的电极反应式CO2+8e-+8H+=CH4+2H2O.
②为提高该人工光合系统的工作效率,可向装置中加入少量硫酸(选填“盐酸”或“硫酸”).
分析 (1)根据①CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H1
②CO(g)+H2O(g)═CO2(g)+H2(g)△H2
③2CO(g)+O2(g)═2CO2(g)△H3
由盖斯定律①+②×2-③×2进行计算得到;
(2)NH4HS中硫元素为-2价,具有还原性能被氧气氧化为硫单质;
(3)①根据化学平衡常数表达的意义书写,利用生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积得到;
②该反应正向为体积增大的方向,压强越大,CH4的转化率越小;压强为P2时,在Y点反应未达到平衡,则反应正向移动;
(4)已知X的相对分子质量为l06,设其分子式为CxHy,由$\frac{106}{12}$可知x=8,y=10,再根据质谱图中有2个峰,判断分子中含有2种环境的H;
(5)①由电池装置图可知,Cu上二氧化碳得电子生成甲烷;
②根据酸的挥发性分析.
解答 解:(1)根据①CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H1
②CO(g)+H2O(g)═CO2(g)+H2(g)△H2
③2CO(g)+O2(g)═2CO2(g)△H3
由盖斯定律①+②×2-③×2得CO2(g)+CH4(g)═2CO(g)+2H2(g)△H=△H1+2△H2-2△H3,故答案为:△H1+2△H2-2△H3;
(2)NH4HS中硫元素为-2价,具有还原性能被氧气氧化为硫单质,则一定条件下向NH4HS溶液中通入空气,得到单质硫和氨水,则反应方程式为:2NH4HS+O2=2NH3•H2O+2S↓;故答案为:2NH4HS+O2=2NH3•H2O+2S↓;
(3)①已知CO2(g)+CH4(g)$\frac{\underline{\;点燃\;}}{\;}$2CO(g)+2H2(g),其平衡常数表达式是K=$\frac{c{\;}^{2}(CO)•c{\;}^{2}(H{\;}_{2})}{c(CO{\;}_{2})•c(CH{\;}_{4})}$,故答案为:K=$\frac{c{\;}^{2}(CO)•c{\;}^{2}(H{\;}_{2})}{c(CO{\;}_{2})•c(CH{\;}_{4})}$;
②该反应正向为体积增大的方向,压强越大,CH4的转化率越小,已知相同温度下,P1条件下的转化率大于P2,则P1小于P2;压强为P2时,在Y点反应未达到平衡,则反应正向移动,所以v(正)大于v(逆);
故答案为:小于;大于;
(4)芳香烃X,已知X的相对分子质量为l06,设其分子式为CxHy,由$\frac{106}{12}$可知x=8,y=10,说明分子中含有一个苯环,另外含有2个C原子,再根据质谱图中有2个峰,可知分子中含有2种环境的H,则分子结构对称,所以其结构简式为 ,故答案为:
,故答案为: ;
;
(5)①由电池装置图可知,Cu上二氧化碳得电子生成甲烷,则Cu电极上的电极反应为:CO2+8e-+8H+=CH4+2H2O,故答案为:CO2+8e-+8H+=CH4+2H2O;
②可向装置中加入少量的酸作电解质,由于盐酸易挥发,生成的甲烷中会混有HCl气体,所以选用硫酸,不用盐酸,故答案为:硫酸.
点评 本题考查了盖斯定律的应用、原电池原理、方程式的书写、化学平衡常数、平衡移动、有机物分子式的确定等,题目涉及的知识点较多,侧重于考查学生对基础知识的综合应用能力,题目难度中等.

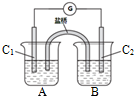
(1)①粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用试剂为:A:盐酸;B:BaCl2溶液;C:NaOH溶液;D:Na2CO3溶液.加入试剂的顺序是CBDA或BCDA.
②电解饱和食盐水时,与电源正极相连的电极上发生的反应为2Cl--2e-=Cl2↑,与电源负极相连的电极附近溶液pH的变化是变大.
(2)工业上从海水中提取的NaCl,可用来制取纯碱,其简要过程如下:向饱和食盐水中先通入气体A,后通入气体B,充分反应后过滤得到晶体C和滤液D,将晶体C灼烧即可制得纯碱,则气体B是CO2(填化学式),由NaCl制取纯碱反应的化学方程为NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl、2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
(3)海水提镁的一段工艺流程如图:
浓海水的主要成分如下:
| 离子 | Na+ | Mg2+ | Cl- | SO42- |
| 浓度/(g•L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
| A. | 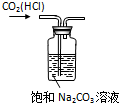 除CO2中的HCl | B. | 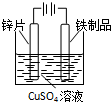 铁制品上镀锌 | C. |  吸收氨气 | D. |  制备少量O2 |
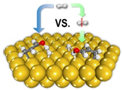 2013年《美国化学会志》发表了我国科学家对非均相催化加氢过程机理研究的成果,其原理如图.下列关于氢气的说法不正确的是( )
2013年《美国化学会志》发表了我国科学家对非均相催化加氢过程机理研究的成果,其原理如图.下列关于氢气的说法不正确的是( )| A. | 由氢原子构成的氢气分子只有一种 | |
| B. | 通常情况下,气体中氢气的密度最小 | |
| C. | 氢气可用于生产盐酸、氨气等化工产品 | |
| D. | 目前,工业上不采用电解水的方法大量生产氢气 |
| A. | XQ2W分子在常温下呈气态,分子中的四个原子在同一平面内 | |
| B. | Z和W形成的两种离子化合物中阴、阳离子个数比均为2:1 | |
| C. | X、W两元素分别和Q元素化合,可形成电子数相同的两种化合物 | |
| D. | 相应的离子半径大小关系为:Y>W>Z |
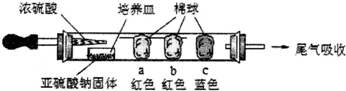
| A. | 本实验是利用强酸制弱酸原理制得SO2气体 | |
| B. | 棉球a沾有品红试液,用以验证SO2的漂白性 | |
| C. | 棉球b红色褪去,说明SO2是酸性氧化物,与水反应能生成亚硫酸 | |
| D. | 棉球C沾有含石蕊的NaOH溶液 |
 已知砷(As)元素的原子结构示意图为
已知砷(As)元素的原子结构示意图为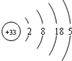
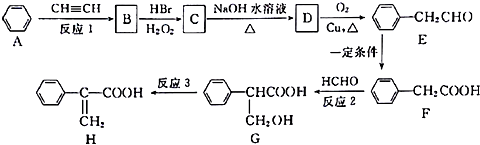
 .
. +NaOH $→_{△}^{水}$
+NaOH $→_{△}^{水}$ +NaBr.
+NaBr. .
.