题目内容
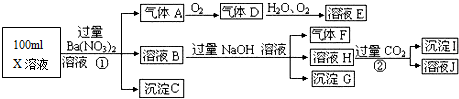
某强酸性溶液X可能含有Ba2+、A13+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42-、C1-、NO3-中的一种或几种,取该溶液进行连续实验,实验过程如下:根据以上信息,回答下列问题:
(1)气体F为 .
(2)上述离子中,溶液X中除H+外还肯定含有的离子是 ,不能确定是否含有的离子是 .
(3)写出生成A的离子方程式: .
(4)通常可以利用KClO在碱性条件下氧化G来制备一种新型、高效、多功能水处理剂K2FeO4.请写出制备过中的离子方程式 .

(1)气体F为
(2)上述离子中,溶液X中除H+外还肯定含有的离子是
(3)写出生成A的离子方程式:
(4)通常可以利用KClO在碱性条件下氧化G来制备一种新型、高效、多功能水处理剂K2FeO4.请写出制备过中的离子方程式
考点:物质的检验和鉴别的实验方案设计,离子共存问题
专题:物质检验鉴别题
分析:强酸性溶液中一定不会存在CO32-和SO32-离子,加入过量硝酸钡生成沉淀,则该沉淀为BaSO4沉淀,说明溶液中含有SO42-离子,生成气体A,A连续氧化生成D和E,则A为NO,D为NO2,E为HNO3,说明溶液中含有还原性离子,一定为Fe2+离子,溶液B中加入过量NaOH溶液,生成气体F,则F为NH3,说明溶液中含有NH4+离子,溶液H中溶于CO2气体,生成沉淀I,则I为Al(OH)3,H为NaAlO2,说明溶液中含有Al3+离子,溶液中含有Fe2+离子,就一定不含NO3-离子,含有SO42-离子就一定不含Ba2+离子,不能确定是否含有的离子Fe3+和Cl-,以此来解答.
解答:
解:强酸性溶液中一定不会存在CO32-和SO32-离子,加入过量硝酸钡生成沉淀,则该沉淀为BaSO4沉淀,说明溶液中含有SO42-离子,生成气体A,A连续氧化生成D和E,则A为NO,D为NO2,E为HNO3,说明溶液中含有还原性离子,一定为Fe2+离子,溶液B中加入过量NaOH溶液,生成气体F,则F为NH3,说明溶液中含有NH4+离子,溶液H中溶于CO2气体,生成沉淀I,则I为Al(OH)3,H为NaAlO2,说明溶液中含有Al3+离子,溶液中含有Fe2+离子,就一定不含NO3-离子,含有SO42-离子就一定不含Ba2+离子,不能确定是否含有的离子Fe3+和Cl-,
(1)由上述分析可知,气体F为NH3,故答案为:NH3;
(2)由上述分析可知,一定含有Al3+、NH4+、Fe2+、SO42-,可能含Fe3+、Cl-,故答案为:Al3+、NH4+、Fe2+、SO42-;Fe3+、Cl-;
(3)A为NO,生成A的离子方程式为3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,故答案为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O;
(4)Fe2+离子被氧化为Fe3+离子,加入NaOH溶液后生成G:Fe(OH)3,和次氯酸反应获得高铁酸钾的方程式为3ClO-+2Fe(OH)3+4OH-═3Cl-+2FeO42-+5H2O,
故答案为:3ClO-+2Fe(OH)3+4OH-═3Cl-+2FeO42-+5H2O.
(1)由上述分析可知,气体F为NH3,故答案为:NH3;
(2)由上述分析可知,一定含有Al3+、NH4+、Fe2+、SO42-,可能含Fe3+、Cl-,故答案为:Al3+、NH4+、Fe2+、SO42-;Fe3+、Cl-;
(3)A为NO,生成A的离子方程式为3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,故答案为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O;
(4)Fe2+离子被氧化为Fe3+离子,加入NaOH溶液后生成G:Fe(OH)3,和次氯酸反应获得高铁酸钾的方程式为3ClO-+2Fe(OH)3+4OH-═3Cl-+2FeO42-+5H2O,
故答案为:3ClO-+2Fe(OH)3+4OH-═3Cl-+2FeO42-+5H2O.
点评:本题考查离子的检验及推断,为高频考点,把握离子之间的反应,转化中气体A、F为解答的关键,侧重分析与推断能力的综合考查,题目难度中等.

练习册系列答案
相关题目
NA表示阿伏加德罗常数,下列说法不正确的是( )
| A、常温常压下,16g O2和16g O3含有的原子数均为NA |
| B、9g重水所含有的电子数为5NA |
| C、100mL 0.1mol/L的Na2SO4溶液中含SO42-的个数为0.01NA |
| D、常温常压下,1mol H2所含的质子数为NA |
山梨酸是一种常用的食品防腐剂,其结构简式如图所示,下列关于山梨酸的说法不正确的是( )


| A、其分子式为C7H10O5 |
| B、分子中含有三种官能团 |
| C、1mol该物质能与3mol NaOH溶液反应 |
| D、能使溴的四氯化碳溶液或酸性高猛酸钾溶液褪色 |

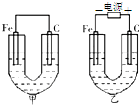 如图所示,甲、乙两池的电极材料都是铁棒与碳棒,请回答:
如图所示,甲、乙两池的电极材料都是铁棒与碳棒,请回答: