题目内容
向100mL 1mol/L的AlCl3溶液中,逐渐滴入2mol/L NaOH溶液,得到3.12g沉淀,则加入的NaOH溶液的体积是多少mL?
考点:化学方程式的有关计算
专题:计算题
分析:100mL 1mol/L的AlCl3溶液中氯化铝的物质的量=0.1L×1mol/L=0.1mol,若Al元素都转化为氢氧化铝沉淀,则氢氧化铝沉淀的质量=0.1mol×78g/mol=7.8g>3.12g,说明有两种情况:一为沉淀不完全,只生成Al(OH)3沉淀;另一种情况为沉淀部分溶解,既生成Al(OH)3沉淀,又生成NaAlO2,结合方程式计算消耗氢氧化钠物质的量,进而计算需要氢氧化钠溶液体积.
解答:
解:100mL 1mol/L的AlCl3溶液中氯化铝的物质的量=0.1L×1mol/L=0.1mol,若Al元素都转化为氢氧化铝沉淀,则氢氧化铝沉淀的质量=0.1mol×78g/mol=7.8g>3.12g,说明有两种情况:一为沉淀不完全,只生成Al(OH)3沉淀;另一种情况为沉淀部分溶解,既生成Al(OH)3沉淀,又生成NaAlO2,
n(Al(OH)3)=
=0.04mol,
①若碱不足,由Al3++3OH-═Al(OH)3↓可知,
NaOH的物质的量为0.04mol×3=0.12mol,
加入NaOH溶液的体积为
=0.06L=60mL;
②沉淀部分溶解,既生成Al(OH)3沉淀,又生成NaAlO2,则:
Al3++3OH-═Al(OH)3↓
0.1mol 0.3mol 0.1mol
Al(OH)3+OH-═AlO2-+2H2O
(0.1-0.04)mol (0.1-0.04)mol
则消耗的碱的物质的量为0.3mol+(0.1-0.04)mol=0.36mol,
加入NaOH溶液的体积为
=0.18L=180mL;
答:加入氢氧化钠溶液的体积为60mL或180mL.
n(Al(OH)3)=
| 3.12g |
| 78g/mol |
①若碱不足,由Al3++3OH-═Al(OH)3↓可知,
NaOH的物质的量为0.04mol×3=0.12mol,
加入NaOH溶液的体积为
| 0.12mol |
| 2mol/L |
②沉淀部分溶解,既生成Al(OH)3沉淀,又生成NaAlO2,则:
Al3++3OH-═Al(OH)3↓
0.1mol 0.3mol 0.1mol
Al(OH)3+OH-═AlO2-+2H2O
(0.1-0.04)mol (0.1-0.04)mol
则消耗的碱的物质的量为0.3mol+(0.1-0.04)mol=0.36mol,
加入NaOH溶液的体积为
| 0.36mol |
| 2mol/L |
答:加入氢氧化钠溶液的体积为60mL或180mL.
点评:本题考查方程式的有关计算,题目难度中等,关键是根据氯化铝与氢氧化铝的量判断发生的反应,再结合反应的有关方程式计算.

练习册系列答案
相关题目
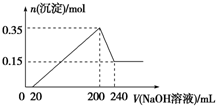 将一定质量的镁和铝混合物投入200mL稀硫酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入的NaOH溶液体积的变化关系如图所示.则下列说法不正确的是( )
将一定质量的镁和铝混合物投入200mL稀硫酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入的NaOH溶液体积的变化关系如图所示.则下列说法不正确的是( )| A、镁和铝的总质量为9g |
| B、合金与稀硫酸反应生成的氢气体积为10.08L |
| C、稀硫酸的物质的量浓度为2.5mol/L |
| D、氢氧化钠溶液的物质的量浓度为5mol/L |
 2013年12月14日,嫦娥三号顺利月面软着陆,月球车表面包裹F46膜,F46膜是由四氟乙烯和全氟丙烯共聚而成.下列有关说法正确的是( )
2013年12月14日,嫦娥三号顺利月面软着陆,月球车表面包裹F46膜,F46膜是由四氟乙烯和全氟丙烯共聚而成.下列有关说法正确的是( )| A、F46膜是纯净物 |
| B、全氟丙烯属于有机物 |
| C、全氟丙烯所有原子共平面 |
| D、四氟乙烯分子中只含非极性键 |

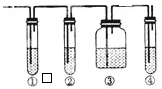 实验室中通常用浓硫酸使乙醇脱水制取少量乙烯,反应机理如为:CH3CH2OH→C2H4↑+H2O.实验中常因温度过高使乙醇与浓硫酸反应生成少量的二氧化硫气体.有人设计了如图的实验,以确定上述混合气体中是否含有乙烯和二氧化硫.
实验室中通常用浓硫酸使乙醇脱水制取少量乙烯,反应机理如为:CH3CH2OH→C2H4↑+H2O.实验中常因温度过高使乙醇与浓硫酸反应生成少量的二氧化硫气体.有人设计了如图的实验,以确定上述混合气体中是否含有乙烯和二氧化硫.