题目内容
甲、乙、丙、丁是四种短周期元素,乙原子有三个电子层,第一层与最外层电子数相等;甲原子的核外电子数比乙原子核外电子数少1;丙原子的最外层电子数是次外层电子数的2倍;丁原子核电荷数比丙原子核电荷数多2.请回答:
(1)甲是 元素(填元素符号),甲的单质与水反应的化学方程式为 ;
(2)乙是 元素(填元素符号),原子结构示意图为 ;
(3)丙是 元素(填元素名称),最高价氧化物对应水化物的化学式是 ;
(4)丁是 元素(填元素名称),甲与丁两种元素可组成的物质有 、 .(填化学式)
(1)甲是
(2)乙是
(3)丙是
(4)丁是
考点:原子结构与元素的性质
专题:元素周期律与元素周期表专题
分析:甲、乙、丙、丁是四种短周期元素,乙原子有三个电子层,第一层与最外层电子数相等,则乙是Mg元素;
甲原子的核外电子数比乙原子核外电子数少1,则甲Na元素;
丙原子的最外层电子数是次外层电子数的2倍,最外层电子数不超过8个,次外层为K层,则丙是C元素;
丁原子核电荷数比丙原子核电荷数多2,则丁是O元素,再结合题目分析解答.
甲原子的核外电子数比乙原子核外电子数少1,则甲Na元素;
丙原子的最外层电子数是次外层电子数的2倍,最外层电子数不超过8个,次外层为K层,则丙是C元素;
丁原子核电荷数比丙原子核电荷数多2,则丁是O元素,再结合题目分析解答.
解答:
解:甲、乙、丙、丁是四种短周期元素,乙原子有三个电子层,第一层与最外层电子数相等,则乙是Mg元素;
甲原子的核外电子数比乙原子核外电子数少1,则甲Na元素;
丙原子的最外层电子数是次外层电子数的2倍,最外层电子数不超过8个,次外层为K层,则丙是C元素;
丁原子核电荷数比丙原子核电荷数多2,则丁是O元素,
(1)甲是Na元素,甲的单质与水反应生成NaOH和氢气,化学方程式为2Na+2H2O=2NaOH+H2↑,故答案为:Na;2Na+2H2O=2NaOH+H2↑;
(2)乙是Mg元素,原子结构示意图为 ,故答案为:Mg;
,故答案为:Mg; ;
;
(3)丙是碳元素,最高价氧化物对应水化物的化学式是H2CO3,故答案为:碳;H2CO3;
(4)丁是氧元素,甲与丁两种元素可组成的物质有Na2O、Na2O2,故答案为:氧;Na2O、Na2O2.
甲原子的核外电子数比乙原子核外电子数少1,则甲Na元素;
丙原子的最外层电子数是次外层电子数的2倍,最外层电子数不超过8个,次外层为K层,则丙是C元素;
丁原子核电荷数比丙原子核电荷数多2,则丁是O元素,
(1)甲是Na元素,甲的单质与水反应生成NaOH和氢气,化学方程式为2Na+2H2O=2NaOH+H2↑,故答案为:Na;2Na+2H2O=2NaOH+H2↑;
(2)乙是Mg元素,原子结构示意图为
 ,故答案为:Mg;
,故答案为:Mg; ;
;(3)丙是碳元素,最高价氧化物对应水化物的化学式是H2CO3,故答案为:碳;H2CO3;
(4)丁是氧元素,甲与丁两种元素可组成的物质有Na2O、Na2O2,故答案为:氧;Na2O、Na2O2.
点评:本题考查了原子结构和元素性质,根据原子结构确定元素,再结合物质的性质分析解答,注意氧化钠、过氧化钠中阴阳离子个数之比都是1:2,为易错点.

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
下列离子方程式书写正确的是( )
| A、向KHSO4溶液中滴入Ba(OH)2溶液使pH=7:SO42-+H++Ba2++OH-=BaSO4↓+H2O |
| B、少量小苏打溶液滴入Ba(OH)2溶液中:HCO3-+Ba2++OH-=BaCO3↓+H2O |
| C、硫氢化钠发生水解:HS-+H2O?H3O++S2- |
| D、FeS固体加入到用硫酸酸化的H2O2溶液中:2Fe2++2H++H2O2=2Fe3++2H2O |
某元素原子核外的电子排布式为1s2…(n-1)d10ns2np2,下列对该元素的判断错误的是( )
| A、一定不是短周期元素 |
| B、可能属于过渡元素 |
| C、一定位于元素周期表的第14列上 |
| D、一定不是非金属元素 |
 (1)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O.已知室温下2g SiH4自燃放出热量89.2kJ.SiH4自燃的热化学方程式为
(1)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O.已知室温下2g SiH4自燃放出热量89.2kJ.SiH4自燃的热化学方程式为
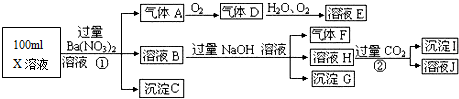
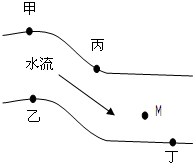 在一条鱼、虾绝迹的小河边有四座工厂甲、乙、丙、丁(如图),它们排出的废液里,每个工厂只有Na2CO3、CuCl2、Ca(OH)2、HCl中的一种.某中学环保小组对河水监测时发现:(1)甲处河水呈乳白色;(2)乙处河水呈浅蓝色浑浊;(3)丙处河水由浑变清;(4)丁处产生气泡,河水仍清.请推断:
在一条鱼、虾绝迹的小河边有四座工厂甲、乙、丙、丁(如图),它们排出的废液里,每个工厂只有Na2CO3、CuCl2、Ca(OH)2、HCl中的一种.某中学环保小组对河水监测时发现:(1)甲处河水呈乳白色;(2)乙处河水呈浅蓝色浑浊;(3)丙处河水由浑变清;(4)丁处产生气泡,河水仍清.请推断: