题目内容
NA表示阿伏加德罗常数,下列说法不正确的是( )
| A、常温常压下,16g O2和16g O3含有的原子数均为NA |
| B、9g重水所含有的电子数为5NA |
| C、100mL 0.1mol/L的Na2SO4溶液中含SO42-的个数为0.01NA |
| D、常温常压下,1mol H2所含的质子数为NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、根据N=n?NA来计算;
B、注意重水的相对分子质量为20,据此来计算;
C、据n=C?V和N=n?NA来计算;
D、1mol H2所含的质子数为2mol.
B、注意重水的相对分子质量为20,据此来计算;
C、据n=C?V和N=n?NA来计算;
D、1mol H2所含的质子数为2mol.
解答:
解:A、16g O2中的氧原子数N1=
×2×NA=NA,16g O3含有的氧原子数N2=
×3×NA=NA,即16g O2和16g O3含有的原子数均为NA,故A正确;
B、重水的相对分子质量为20,9g重水含有的电子数为
×10×NA=4.5NA,故B错误;
C、n(SO42-)=C?V=0.1mol/L×0.1L=0.01mol,个数为0.01NA个,故C正确;
D、1mol H2所含的质子数为2mol,即2NA个,故D正确.
故选B.
| 16g |
| 32g/mol |
| 16g |
| 48g/mol |
B、重水的相对分子质量为20,9g重水含有的电子数为
| 9g |
| 20g/mol |
C、n(SO42-)=C?V=0.1mol/L×0.1L=0.01mol,个数为0.01NA个,故C正确;
D、1mol H2所含的质子数为2mol,即2NA个,故D正确.
故选B.
点评:本题考查了有关阿伏伽德罗常数的有关计算,熟练掌握公式和物质的结构特点是关键.

练习册系列答案
相关题目
皮肤上沾了少量苯酚,正确的处理方法是( )
| A、先用稀NaOH溶液洗,再用水冲洗 |
| B、先用水洗,再用酒精冲洗 |
| C、先用酒精洗,再用水冲洗 |
| D、用布擦去后再用水冲洗 |
下列离子方程式书写正确的是( )
| A、向KHSO4溶液中滴入Ba(OH)2溶液使pH=7:SO42-+H++Ba2++OH-=BaSO4↓+H2O |
| B、少量小苏打溶液滴入Ba(OH)2溶液中:HCO3-+Ba2++OH-=BaCO3↓+H2O |
| C、硫氢化钠发生水解:HS-+H2O?H3O++S2- |
| D、FeS固体加入到用硫酸酸化的H2O2溶液中:2Fe2++2H++H2O2=2Fe3++2H2O |
在100mL 1.0mol/L的AlCl3溶液中加入350mL 1.0mol/L的NaOH溶液充分反应后,得到的沉淀的质量是( )
| A、7.8g | B、3.9g |
| C、15.6g | D、无沉淀 |
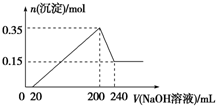 将一定质量的镁和铝混合物投入200mL稀硫酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入的NaOH溶液体积的变化关系如图所示.则下列说法不正确的是( )
将一定质量的镁和铝混合物投入200mL稀硫酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入的NaOH溶液体积的变化关系如图所示.则下列说法不正确的是( )| A、镁和铝的总质量为9g |
| B、合金与稀硫酸反应生成的氢气体积为10.08L |
| C、稀硫酸的物质的量浓度为2.5mol/L |
| D、氢氧化钠溶液的物质的量浓度为5mol/L |
下列各组离子在给定条件下能大量共存的是( )
| A、能使pH试纸呈红色的溶液:Na+、NH4+、Cl-、NO3- |
| B、滴入KSCN溶液显血红色的溶液:K+、Na+、CO32-、I- |
| C、能与铝反应产生H2的溶液:K+、Fe2+、Cl-、NO3- |
| D、常温下由水电离出的c(H+)=1×10-13mol/L的溶液:HCO3-、K+、SO42-、Cl- |
某元素原子核外的电子排布式为1s2…(n-1)d10ns2np2,下列对该元素的判断错误的是( )
| A、一定不是短周期元素 |
| B、可能属于过渡元素 |
| C、一定位于元素周期表的第14列上 |
| D、一定不是非金属元素 |
 (1)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O.已知室温下2g SiH4自燃放出热量89.2kJ.SiH4自燃的热化学方程式为
(1)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O.已知室温下2g SiH4自燃放出热量89.2kJ.SiH4自燃的热化学方程式为