题目内容
14.25℃时,pH=12的NaOH溶液100mL,要使它的pH为11.(溶液体积变化忽略不计)(1)如果加入蒸馏水,应加900mL;
(2)如果加入pH=10的NaOH溶液,应加1000mL;
(3)如果加0.01mol/L HCl,应加81.8mL.(精确到0.1)
分析 (1)先根据溶液的pH计算氢氧根离子浓度,再根据c1V1=c2(V1+V2)计算加入的水体积;
(2)先根据溶液的pH计算氢氧根离子浓度,再根据c1V1+c2V2=c3(V1+V2)计算加入的氢氧化钠溶液体积;
(3)先计算混合溶液中氢氧根离子浓度,再根据c(OH-)=$\frac{n(碱)-n(酸)}{V(酸)+V(碱)}$计算.
解答 解:(1)pH=12 的NaOH溶液中氢氧根离子浓度是0.01mol/L,pH=11的氢氧化钠溶液中氢氧根离子浓度是0.001mol/L,设加入水的体积是V2,c1V1=c2(V1+V2)=0.01mol/L×0.1L=(0.1+V2)L×0.001mol/L,则:V2=$\frac{0.01mol/L×0.1L}{0.001mol/L}$=0.9L=900mL,
故答案为:900;
(2)pH=12 的NaOH溶液中氢氧根离子浓度是0.01mol/L,pH=11的氢氧化钠溶液中氢氧根离子浓度是0.001mol/L,pH=10的氢氧化钠溶液中氢氧根离子浓度是0.0001mol/L,
设加入pH=10的NaOH溶液体积是V2,c1V1+c2V2=c3(V1+V2)=0.01mol/L×0.1L+0.0001mol/L×V2=0.001mol/L(0.1+V2),
解得:V2=1L=1000mL,
故答案为:1000;
(3)盐酸的浓度是0.01mol/L,设加入盐酸的体积是V,c(OH-)=$\frac{n(碱)-n(酸)}{V(酸)+V(碱)}$=$\frac{0.01mol/L×0.1L-0.01mol/L×VL}{(0.1+V)L}$=0.001mol/L,
解得:V=81.8mL,
故答案为:81.8.
点评 本题考查了酸碱混合的定性判断及溶液pH的计算,题目难度中等,明确溶液pH的计算方法为解答关键,试题侧重考查学生达到分析、理解能力及化学计算计算能力.

| A. | 锂与水反应不如钠与水反应剧烈 | |
| B. | 还原性:K>Na>Li,故K可以从NaCl溶液中置换出金属钠 | |
| C. | 熔沸点:Li>Na>K | |
| D. | 原子半径:Li<Na<K |
| A. | 氮分子的结构式:N-N | B. | Mg2+的结构示意图: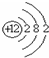 | ||
| C. | 二氧化碳电子式 | D. | 钙离子的电子式:Ca2+ |
(1)以氨为燃料可以设计制造氨燃料电池,因产物无污染,在很多领域得到广泛应用.若电极材料均为惰性电极,KOH溶液作电解质溶液,则该电池负极电极反应式为2NH3-6e-+6OH-=N2+6H2O.
(2)在一定温度下,在固定体积的密闭容器中进行可逆反应:N2+3H2?2NH3.该可逆反应达到平衡的标志是BCE.
A.3v(H2)正=2v(NH3)逆
B.单位时间生成m mol N2的同时消耗3m mol H2
C.容器内的总压强不再随时间而变化
D.混合气体的密度不再随时间变化
E.a molN≡N键断裂的同时,有6amolN-H键断裂
F.N2、H2、NH3的分子数之比为1:3:2
(3)某化学研究性学习小组模拟工业合成氨的反应.在容积固定为2L的密闭容器内充入1molN2和3molH2,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,并用压力计监测容器内压强的变化如下:
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 压强/MPa | 16.80 | 14.78 | 13.86 | 13.27 | 12.85 | 12.60 | 12.60 |
(4)以CO2与NH3为原料合成尿素[化学式为CO(NH2)2]的主要反应如下,已知:
①2NH3(g)+CO2(g)═NH2CO2NH4(s)△H=-l59.5kJ•mol-1
②NH2CO2NH4(s)?CO(NH2)2(s)+H2O(g)△H=+116.5kJ•mol-1
③H2O(1)═H2O(g)△H=+44.0kJ•mol-1
写出CO2与NH3合成尿素和液态水的热化学反应方程式2NH3(g)+CO2(g)═CO(NH2)2(s)+H2O(l)△H=-87.0kJ•mol-1;
对于上述反应②在密闭容器中将过量NH2CO2NH4固体于400K下分解,平衡时体系压强为a Pa,若反应温度不变,将体系的体积增加50%,则体系的压强是a Pa(用含a的式子表示).
①硒位于周期表第4周期,VIA族;
②硒的最高价氧化物的化学式为SeO3,对应水化物的化学式为H2SeO4;
(2)如表是某一周我国部分城市空气质量周报,阅读并回答下列问题.
| 城市 | 污染指数 | 首要污染物 | 空气质量级别 |
| 北京 | 92 | TSP | Ⅱ |
| 上海 | 74 | Ⅱ | |
| 济南 | 76 | TSP | Ⅱ |
| 重庆 | 98 | Ⅱ |
②二氧化硫是常见的大气污染物之一,我国规定空气中二氧化硫含量不得超过0.02mg/L.为减少二氧化硫排放量,下列措施中,可采取的是AB.
A.用天然气代替煤炭做民用燃料
B.采用燃料脱硫技术
C.向已酸化的土壤中加石灰
D.植树造林.
| A. | 氯化氢比硫化氢稳定 | B. | 次氯酸的氧化性比硫酸强 | ||
| C. | 高氯酸的酸性比硫酸的强 | D. | 氯气能与硫化氢反应生成硫 |
| A. | 地球上绝大多数金属元素是以游离态存在于自然界中的 | |
| B. | 在化学反应中,金属容易失去电子,是还原剂 | |
| C. | 多数合金的熔点高于组成它的成分的金属的熔点 | |
| D. | 硅单质是良好的半导体,所以它是金属元素 |
| A. | pH=12的氢氧化钠溶液与pH=2的某酸溶液等体积混合 | |
| B. | pH=2的某酸溶液与pH=12某碱溶液等体积混合 | |
| C. | pH=2的盐酸pH=12的氨水等体积混合 | |
| D. | 1×10-3mol/L的盐酸和6×10-4mol/L的Ba(OH)2溶液各取10mL,混合后再稀释100倍 |
 .
. .
.