题目内容
3.在人类社会的发展进程中,金属起着重要的作用.下列说法正确的是( )| A. | 地球上绝大多数金属元素是以游离态存在于自然界中的 | |
| B. | 在化学反应中,金属容易失去电子,是还原剂 | |
| C. | 多数合金的熔点高于组成它的成分的金属的熔点 | |
| D. | 硅单质是良好的半导体,所以它是金属元素 |
分析 A.多数金属性质活泼,容易被氧化;
B.失去电子发生氧化反应,做还原剂;
C.合金的熔点低于组成合金成分金属的熔点;
D.硅为非金属元素.
解答 解;A.多数金属性质活泼,容易被氧化,在自然界中以化合态存在,故A错误;
B.在化学反应中,金属容易失去电子,是还原剂,故B正确;
C.多数合金的熔点低于组成它的成分的金属的熔点,故C错误;
D.硅单质是良好的半导体,导电性介于导体与绝缘体之间,它是非金属元素,故D错误;
故选:B.
点评 本题考查了元素在自然界中存在形态、合金性质、硅的性质,题目难度不大,熟悉合金熔点低于成分金属熔点是解题关键.

练习册系列答案
相关题目
2.下列装置或操作能达到实验目的是( )
| A. |  实验室制取并收集NH3 | B. | 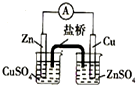 构成原电池 | ||
| C. | 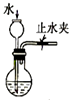 检查装置气密性 | D. |  利用排空气法收集CO2 |
11.下列有机物中,不属于烃的衍生物的是( )
| A. | 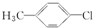 | B. | CH3CH2NO2 | C. | CH2=CHBr | D. | CΗ3-CH3 |
18.有4组同一族元素所形成的不同物质,在101kPa时测定它们的沸点(℃)如表所示,则下列各项判断正确的是( )
| 第一组 | He | -268.8 | (a) | -249.5 | Ar | -185.8 | Kr | -151.7 |
| 第二组 | F2 | -187.0 | Cl2 | -33.6 | (b) | 58.7 | I2 | 184.0 |
| 第三组 | (c) | 19.4 | HCl | -84.0 | HBr | -67.0 | HI | -35.3 |
| 第四组 | H2O | 100.0 | H2S | -60.2 | (d) | -42.0 | H2Te | -1.8 |
| A. | abc的化学式分别为Ne2、Br2、HF | |
| B. | 第三组与第四组相比较,化合物的稳定顺序为:HBr<d | |
| C. | 第三组物质溶于水后,溶液的酸性c最强 | |
| D. | 第四组物质中H2O的沸点最高,是因为H2O分子内存在氢键 |
15.某同学设计如下元素周期表,以下说法正确的是( )
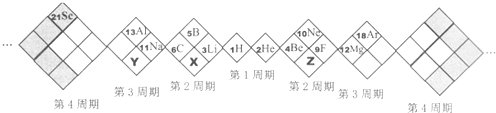

| A. | X、Y、Z元素分别为N、P、O | B. | 所列元素都是主族元素 | ||
| C. | 原子半径:Z>X>Y | D. | 稳定性:X的氢化物<Y的氢化物 |
13.国际奥委会于2010年2月10日宣布,有30名运动员兴奋剂药检呈阳性,被取消参加2010年温哥华冬季奥运会的资格.以下是其中检测出的两种兴奋剂的分子结构:

关于它们的说法中正确的是( )

关于它们的说法中正确的是( )
| A. | X能发生取代反应、酯化反应、加成反应和水解反应 | |
| B. | Y分子中的所有碳原子不可能共平面 | |
| C. | X、Y均能与溴水反应 | |
| D. | X、Y均能与饱和碳酸钠溶液反应放出CO2 |
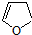 ,顺丁烯二酸酐
,顺丁烯二酸酐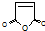 等药物中间体,广泛用于涂料行业的顺丁烯二酸二甲酯其合成流程图如下:
等药物中间体,广泛用于涂料行业的顺丁烯二酸二甲酯其合成流程图如下: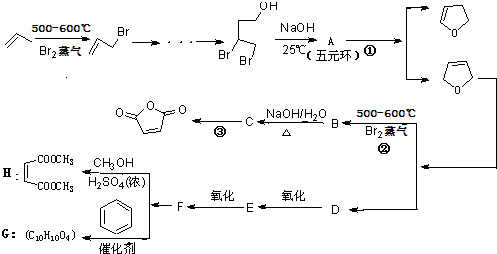
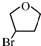 .D的结构简式HOCH2CH=CHCH2OH
.D的结构简式HOCH2CH=CHCH2OH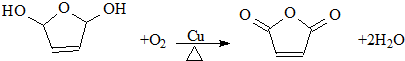 .
.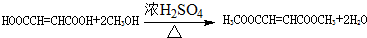 .
.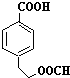 、
、 .
.