题目内容
【题目】常温下,浓度均为![]() 的
的![]() 溶液和HCN溶液的pH分别为m和
溶液和HCN溶液的pH分别为m和![]() 下列叙述中不正确的是
下列叙述中不正确的是
A.HCN溶液和NaOH溶液不等体积混合后一定存在![]()
B.等温下,等浓度的![]() 溶液和NaCN溶液的pH,后者大
溶液和NaCN溶液的pH,后者大
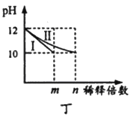
C.常温下,pH相同的![]() 溶液和HCN溶液分别加水稀释相同的倍数时,前者pH的变化小
溶液和HCN溶液分别加水稀释相同的倍数时,前者pH的变化小
D.溶液中由水电离出的![]() ,前者是后者的
,前者是后者的![]() 倍
倍
【答案】C
【解析】
常温下,等物质的量浓度的醋酸和氢氰酸,氢氰酸的pH大于醋酸,说明醋酸的酸性大于氢氰酸,据此分析解答。
A、根据电荷守恒知,![]() ,所以得
,所以得![]() ,故A正确;
,故A正确;
B、等温下,等浓度的![]() 溶液和NaCN溶液中NaCN的水解程度大,溶液的碱性强,pH大,故B正确;
溶液和NaCN溶液中NaCN的水解程度大,溶液的碱性强,pH大,故B正确;
C、等pH的两种酸,稀释相同的倍数,弱酸的pH变化小于强酸,所以pH相同的![]() 溶液和HCN溶液分别加水稀释相同的倍数时,前者pH变化较大,故C错误;
溶液和HCN溶液分别加水稀释相同的倍数时,前者pH变化较大,故C错误;
D、酸溶液中由水电离出的氢离子浓度等于溶液中氢氧根离子浓度,![]() 和HCN溶,醋酸溶液中由水电离出的
和HCN溶,醋酸溶液中由水电离出的![]() ,氢氰酸溶液中由水电离出的
,氢氰酸溶液中由水电离出的![]() ,所以前者是后者的
,所以前者是后者的![]() 倍,故D正确;
倍,故D正确;
故选C。

练习册系列答案
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案
相关题目
【题目】已知:Fe2+遇铁氰化钾(K3[Fe(CN)6])会产生特征的蓝色沉淀;AgI是难溶于水的黄色固体。将0.2mol·L-1的KI溶液和0.05mol·L-1Fe2(SO4)3溶液等体积混合后,取混合液分别完成上述实验,能说明溶液中存在化学平衡“2Fe3++2I-![]() 2Fe2++I2”的是( )
2Fe2++I2”的是( )
编号 | 实验操作 | 实验现象 |
① | 滴入KSCN溶液 | 溶液变红色 |
② | 滴入AgNO3溶液 | 生成黄色沉淀 |
③ | 滴入K3[Fe(CN)6]溶液 | 生成蓝色沉淀 |
④ | 滴入淀粉溶液 | 溶液变蓝色 |
A.①B.②和④C.③和④D.③