题目内容
【题目】某学习小组按如下实验流程探究海带中碘含量的测定和碘的制取。

(实验一)碘含量的测定。取0.0100mol/L的AgNO3标准溶液装入滴定管,取100.00mL海带浸取原液至滴定池,用电势滴定法测定碘含量。测得的电动势(E)反映溶液中c(I-)的变化,部分数据如下表:
V(AgNO3)/mL | 15.00 | 19.00 | 19.80 | 19.98 | 20.00 | 20.02 | 21.00 | 23.00 | 25.00 |
E/mV | -225 | -200 | -150 | -100 | 50.0 | 175 | 275 | 300 | 325 |
回答下列问题:
(1)实验中“灼烧”是在__(填仪器名称)中完成的。
(2)用文字具体描述“定容”过程:__
(3)根据表中数据判断滴定终点时用去AgNO3溶液的体积为__mL,计算得海带中碘的质量百分含量为__%。
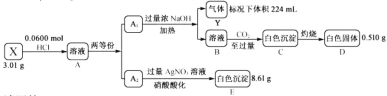
(实验二)碘的制取。另制海带浸取原液,甲、乙两种实验方案如下:

已知:3I2+6NaOH=5NaI+NaIO3+3H2O。
(4)“适量O2”中能代替O2的最佳物质对应的电子式为__
(5)若要测定“I2+水溶液”中碘的含量,可以选择__作指示剂,用Na2S2O3溶液滴定,滴定终点的现象是__。
(6)若得到“I2+水溶液”时加入硫酸溶液过多,用Na2S2O3溶液滴定时会产生明显的误差,产生此误差的原因为__(用离子方程式表示)。
【答案】坩埚 容量瓶中加蒸馏水至刻度线下1~2cm处,改用胶头滴管滴加蒸馏水至凹液面最低处与刻度线相切 20.00 0.635 ![]() 淀粉溶液 滴加最后一滴Na2S2O3溶液时,锥形瓶内的溶液由蓝色变为无色,且半分钟内不变色 2H++
淀粉溶液 滴加最后一滴Na2S2O3溶液时,锥形瓶内的溶液由蓝色变为无色,且半分钟内不变色 2H++![]() =S↓+SO2↑+H2O
=S↓+SO2↑+H2O
【解析】
本实验为探究海带中碘含量的测定和碘的制取实验,碘含量的测定实验中,将干海带在坩埚中灼烧后加水溶解、转移,煮沸、过滤、转移到定容容器中得到含有I-的海带浸取原液,用AgNO3的标准溶液进行滴定,根据关系式法求得海带中碘的质量百分含量;碘的制取实验中,向海带浸取原液中通入适量的O2将I-氧化为I2,再用CCl4萃取分液后得到含有I2的CCl4溶液,经蒸馏(方案甲)可得到纯碘,或加入NaOH溶液,发生反应3I2+6NaOH=5NaI+NaIO3+3H2O,分液后向上层液体中加入H2SO4,I-和![]() 发生归中反应得到I2+水溶液,再经一系列步骤得到纯碘,据此分析解答问题。
发生归中反应得到I2+水溶液,再经一系列步骤得到纯碘,据此分析解答问题。
【实验一】
(1)实验中“灼烧”一般在坩埚中进行,则进行灼烧的仪器名称为坩埚;
(2)根据配制一定物质的量浓度溶液定容操作为:继续向容量瓶中加蒸馏水至刻度线下1~2cm处,改用胶头滴管滴加蒸馏水至凹液面最低处与刻度线相切;
(3)利用硝酸银溶液滴定碘离子,根据表格中电动势的变化可得,当加入硝酸银溶液的体积为19.98~20.02mL之间时,电动势发生突变,则滴定终点时用去AgNO3溶液的体积为20.00mL,则碘的百分含量为![]() ×100%=0.635%;
×100%=0.635%;
【实验二】
(4)向含有碘离子的海带浸取原液通入适量氧气将碘离子氧化为碘单质,可用其他氧化剂来氧化碘离子且不引入新的杂质,可以选用双氧水来作氧化剂氧化碘离子,双氧水的电子式为![]() ;
;
(5)碘单质遇淀粉变蓝,则滴定操作可用淀粉溶液作指示剂,滴定终点时,碘单质被Na2S2O3溶液全部转化为碘离子,现象为:滴加最后一滴Na2S2O3溶液时,锥形瓶内的溶液由蓝色变为无色,且半分钟内不变色;
(6)酸性条件下,Na2S2O3自身会发生歧化反应,离子反应方程式为:2H++![]() =S↓+SO2↑+H2O。
=S↓+SO2↑+H2O。

 阅读快车系列答案
阅读快车系列答案