题目内容
14.化合物A(C10H12O2)经碱性水解,酸化后得到B和C8H8O2,C经现代物理方法证明含有苯环,且苯环上有2种氢原子;D为甲醛的同系物,相同条件下其蒸气与氢气的密度比为22.C可以经过反应合成香料I: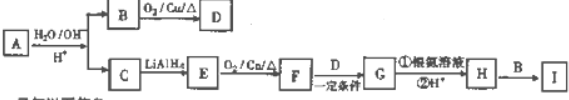
已知以下信息:
①RCHO+R′CH2CHO$\stackrel{一定条件}{→}$
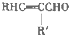 +H2O
+H2O②RCHO$\stackrel{LiAl{H}_{4}}{→}$RCH2OH
请回答下列问题:
(1)B的结构式是CH3CH2OH;C中官能团的名称是羧基.
(2)E的名称为对甲基苯甲醇.
(3)H和B反应生成I的化学方程式为
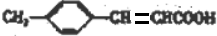 +CH3CH2OH$→_{△}^{浓硫酸}$
+CH3CH2OH$→_{△}^{浓硫酸}$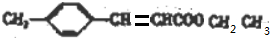 +H2O,反应类型为取代反应(酯化反应).
+H2O,反应类型为取代反应(酯化反应).(4)满足下列条件的C的所有同分异构体共有3种(不考虑立体异构),其中核磁共振氢谱有4组峰,且峰面积比为3:2:2:1的为
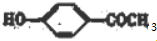 (写结构简式).
(写结构简式).①是苯的对位二取代化合物;
②能与FeCl3溶液发生显色反应;
③不考虑烯醇(
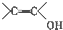 )结构.
)结构.
分析 化合物A(C12H12O2)经碱性水解、酸化后得到B和C(C8H8O2),B能二次氧化生成D,说明A是酯,B是醇,则C是羧酸,C(C8H8O2)的核磁共振氢谱表明含有苯环,且苯环上有2种氢原子,则说明苯环上有2个取代基,且两个取代基处于对位,根据C的分子式知,C是对甲基苯甲酸,则C是羧酸,C(C8H8O2)的核磁共振氢谱表明含有苯环,且苯环上有2种氢原子,则说明苯环上有2个取代基,且两个取代基处于对位,根据C的分子式知,C是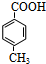 ,化合物A(C12H12O2),A是酯,B是醇,
,化合物A(C12H12O2),A是酯,B是醇,
则A→B+C: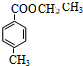 +H2O$\stackrel{OH-}{→}$CH3CH2OH+
+H2O$\stackrel{OH-}{→}$CH3CH2OH+
B→D:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O
C→E: $\stackrel{LIAlH_{4}}{→}$
$\stackrel{LIAlH_{4}}{→}$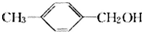
E→F:2 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2 +2H2O
+2H2O
F+D→G: +CH3CHO$\stackrel{一定条件}{→}$
+CH3CHO$\stackrel{一定条件}{→}$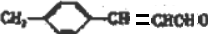 +H2O
+H2O
G→H: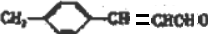 +2Ag(NH3)2OH$\stackrel{水浴}{→}$
+2Ag(NH3)2OH$\stackrel{水浴}{→}$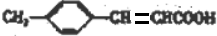 +2Ag↓+H2O+4NH3;
+2Ag↓+H2O+4NH3;
H+B→I: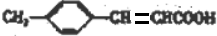 +CH3CH2OH$→_{△}^{浓硫酸}$
+CH3CH2OH$→_{△}^{浓硫酸}$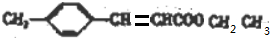 +H2O,据此分析解答.
+H2O,据此分析解答.
解答 解:(1)化合物A(C12H12O2)经碱性水解、酸化后得到B和C(C8H8O2),B能二次氧化生成D,说明A是酯,B是醇,则C是羧酸,C(C8H8O2)的核磁共振氢谱表明含有苯环,且苯环上有2种氢原子,则说明苯环上有2个取代基,且两个取代基处于对位,根据C的分子式知,C是对甲基苯甲酸,则C是羧酸,C(C8H8O2)的核磁共振氢谱表明含有苯环,且苯环上有2种氢原子,则说明苯环上有2个取代基,且两个取代基处于对位,根据C的分子式知,C是 ,化合物A(C12H12O2),A是酯,B是醇,
,化合物A(C12H12O2),A是酯,B是醇,
则A→B+C: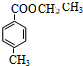 +H2O$\stackrel{OH-}{→}$CH3CH2OH+
+H2O$\stackrel{OH-}{→}$CH3CH2OH+ ,B为CH3CH2OH,C为
,B为CH3CH2OH,C为 ,C中官能团的名称是羧基,
,C中官能团的名称是羧基,
故答案为:CH3CH2OH;羧基;
(2)C→E: $\stackrel{LIAlH_{4}}{→}$
$\stackrel{LIAlH_{4}}{→}$ ,苯环对位上有两个取代基,1个甲基,一个醇羟基,所以E为对甲基苯甲醇,
,苯环对位上有两个取代基,1个甲基,一个醇羟基,所以E为对甲基苯甲醇,
故答案为:对甲基苯甲醇;
(3)H+B→I: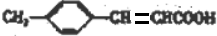 +CH3CH2OH$→_{△}^{浓硫酸}$
+CH3CH2OH$→_{△}^{浓硫酸}$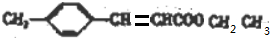 +H2O,反应本质为酸脱羟基醇脱氢,为取代反应(酯化反应),
+H2O,反应本质为酸脱羟基醇脱氢,为取代反应(酯化反应),
故答案为: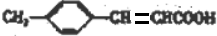 +CH3CH2OH$→_{△}^{浓硫酸}$
+CH3CH2OH$→_{△}^{浓硫酸}$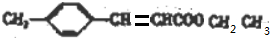 +H2O;取代反应(酯化反应);
+H2O;取代反应(酯化反应);
(4)C是 ,C的同分异构体,①是苯的对位二取代化合物,说明含有2个取代基,
,C的同分异构体,①是苯的对位二取代化合物,说明含有2个取代基,
②能与FeCl3溶液发生显色反应,说明含有酚羟基;
③不考虑烯醇( )结构,符合条件的异构体有:
)结构,符合条件的异构体有: 、
、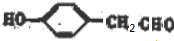 、
、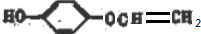 苯环上有2种氢原子;其中核磁共振氢谱为4组峰,且面积比为3:2:2:1,说明含有1个-CH3,符合条件的为
苯环上有2种氢原子;其中核磁共振氢谱为4组峰,且面积比为3:2:2:1,说明含有1个-CH3,符合条件的为 ,
,
故答案为:3; .
.
点评 本题考查有机物的推断,题目难度较大,明确有机物的种类为解答该题的关键,注意结合题给信息、反应流程中官能团的变化判断.

 阅读快车系列答案
阅读快车系列答案| A. | 将SO2气体通入NaClO溶液中:SO2+ClO-+H2O=SO32-+2HClO | |
| B. | 向FeBr2溶液中通入过量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | |
| C. | 三氯化铝溶液与足量的氨水反应:Al3++4OH-=[Al(OH)4]- | |
| D. | 用三氯化铁溶液腐蚀铜印刷电路板:2Fe3++Cu=Cu2++2Fe2+ |
| A. | 中性溶液中可能大量存在:Ca2+,Cl-,SO42-,K+ | |
| B. | 弱酸性溶液中可能大量存在:Cu2+,NH4+,NO3-,Cl- | |
| C. | 使石蕊试液变蓝的溶液中可能大量存在:Na+,Al3+,SO42-,NO3- | |
| D. | 水电离的c(OH-)=10-10mol/L溶液中可能大量存在:l-,NO3-,Mg2+,K+ |
| A. | 铝合金熔点低,可用来制造门窗 | |
| B. | 二氧化氯具有强氧化性,可用来漂白织物 | |
| C. | 过氧化钠固体呈淡黄色,可用来做供氧剂 | |
| D. | 硫酸铜溶于水呈酸性,可用来做杀菌剂 |
| A. | 将2mol Cl2通入到含1mol FeBr2的溶液中:2Fe2++2Br-+2Cl2═2Fe3++4Cl-+Br2正确;Cl2过量,Fe2+、Br-均被氧化 | |
| B. | 用Cu电极电解NaCl溶液阳极的电极反应式:2Cl--2e-═Cl2↑正确;Cl-优先于OH-放电 | |
| C. | 过量SO2通入到NaClO溶液中:SO2+H2O+ClO-═HClO+HSO3-正确;H2SO3的酸性强于HClO | |
| D. | Mg(HCO3)2溶液与足量的NaOH溶液反应:Mg2++2HCO3-+4OH-═Mg(OH)2↓+2CO32-+2H2O正确;Mg(OH)2比MgCO3更难溶 |
| A. | pH=4的CH3COOH溶液加水稀释10倍,溶液中各离子浓度均减小 | |
| B. | 用CH3COOH溶液滴定等浓度的NaOH至pH=7,V(CH3COOH溶液)<V(NaOH溶液) | |
| C. | 向0.2moj/L的盐酸中加入等体积0.1mol/L氨水溶液:c(Cl-)+c(OH-)=c(H+)+c(NH3••H2O) | |
| D. | 在含0.1mol NaHSO4溶液中:c(H+)=c(SO42-)+c(OH-) |
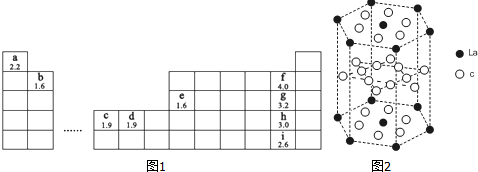
(1)b、h两元素可形成化合物bh2,写出其电子式:
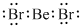 .
.(2)e、g两元素可形成两种化合物eg3、e2g6,eg3的分子构型为平面正三角形,eg3、e2g6中心原子e的杂化方式分别为sp2、sp3.
(3)d元素形成的单质可与g的氢化物浓溶液在加热条件下反应生成一种以二价d离子为内界中心原子(配位数为4)的配位化合物与一种可燃性气体,写出反应的化学方程式:Cu+4HCl=H2CuCl4+H2↑.
(4)f、g、h、i四种元素对应单质分子的键能如下表:
| 共价键 | f-f | g-g | h-h | i-i |
| 键能(kJ/mol) | 157 | 242.7 | 193.7 | 152.7 |
(5)c元素的元素符号是Ni,价电子排布式为3d84s2,下图是一种受到较多关注的c元素单质与金属镧(La)形成的储氢材料的结构示意图,请在图2中勾画出该晶体的一个晶胞.计算出该合金的化学式为:LaNi5.