题目内容
反应NH4HS(s)?NH3(g)+H2S(g)在某一温度下达到平衡,下列各种情况中,能使化学平衡发生移动的是( )
| A、减少部分NH4HS固体 |
| B、压强、温度不变,充入少量氩气 |
| C、容积、温度一定,充入氦气 |
| D、温度、容积一定,充入SO2气体 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:A、硫氰化铵是固体,不影响化学平衡;
B、固体不影响化学平衡;
C、充入稀有气体,各组分浓度没有变化,化学平衡不移动;
D、充入二氧化硫,二氧化硫能够与氯化氢反应,导致硫化氢浓度降低.
B、固体不影响化学平衡;
C、充入稀有气体,各组分浓度没有变化,化学平衡不移动;
D、充入二氧化硫,二氧化硫能够与氯化氢反应,导致硫化氢浓度降低.
解答:
解:A、由于硫氰化铵是固体,不影响化学平衡,故A错误;
B、压强温度一定,充入少量氩气,体积增大,压强减小,平衡 正向进行,故B正确;
C、容积、温度一定,充入氦气,各组分的浓度没有发生变化,化学平衡不移动,故C错误;
D、温度、容积一定,充入SO2气体,由于二氧化硫能够与硫化氢反应,导致反应物浓度减小,化学平衡向着正向移动,故D正确;
故选BD.
B、压强温度一定,充入少量氩气,体积增大,压强减小,平衡 正向进行,故B正确;
C、容积、温度一定,充入氦气,各组分的浓度没有发生变化,化学平衡不移动,故C错误;
D、温度、容积一定,充入SO2气体,由于二氧化硫能够与硫化氢反应,导致反应物浓度减小,化学平衡向着正向移动,故D正确;
故选BD.
点评:本题考查了化学平衡的影响因素,注意恒容、恒温体积下充入稀有气体,化学平衡不移动,本题难度中等.

练习册系列答案
相关题目
现用氯水来制取含有次氯酸的溶液,既要提高溶液中HClO物质的量浓度,又要降低溶液中HCl浓度,下列措施可以采用的是( )
| A、加热挥发HCl |
| B、加水使平衡向正反应方向移动 |
| C、加NaOH中和HCl |
| D、加CaCO3中和HCl |
下列离子方程式正确的是( )
| A、Ca(HCO3)2溶液中加入足量的Ba(OH)2溶液Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O |
| B、向小苏打溶液中加入醋酸溶液:HCO3-+H+═CO2↑+H2O |
| C、碳酸钡与硫酸反应:Ba2++SO42-═BaSO4↓ |
| D、向NH4HSO4稀溶液中逐滴加入Ba(OH)2溶液至刚好沉淀完全NH4++H++SO42-+Ba2++2OH-═NH3?H2O+BaSO4↓+H2O |
已知+4价的S元素具有较强的还原性,某溶液中含有HCO3-、SO32-、CO32-、Cl-等4种阴离子.向其中加入足量的Na2O2固体后,溶液中离子浓度基本保持不变的是(假设溶液体积无变化)( )
| A、CO32- |
| B、SO32- |
| C、Cl- |
| D、HCO3- |
下列叙述与对应图式正确的是( )
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径 | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 主要化合价 | -2 | +2 | +1 | +5、-3 | +7、-1 | +1 | +5、-3 | +3 |
| A、由下列短周期元素性质的数据推断元素③最高价氧化物对应的水化物碱性最强 |
B、 如图装置中,待镀铁制品应与电源负极相连 |
C、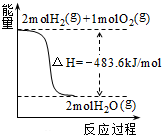 如图表示H2与O2发生反应过程中的能量变化,则H2的燃烧热的热化学方程式为:2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ/mol |
D、 如图表示某一放热反应,若使用催化剂E1、E2、△H都会发生改变 |
将0.01mol的下列物质分别加入(或通入)到100mL水中,假设溶液体积变化不计,水溶液的导电能力最强的是( )
| A、HF |
| B、NH4HCO3 |
| C、BaSO4 |
| D、NH3 |
某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2,已知该反应中H2O2只发生如下过程:H2O2→O2.则下列说法中正确的是( )
| A、上述过程的氧化剂为H2O2 | ||
B、若上述过程中产生的氧气为1mol,则消耗的H2CrO4为
| ||
| C、上述过程中Cr(OH)3是反应物 | ||
| D、上述过程的氧化产物为H2CrO4 |
将2.4mol某金属投入1.8L 2mol/L的某酸溶液中,恰好完全反应,并产生7.2g氢气,则该金属和酸分别是( )
| A、二价金属,二元酸 |
| B、二价金属,三元酸 |
| C、三价金属,二元酸 |
| D、一价金属,一元酸 |