题目内容
将0.01mol的下列物质分别加入(或通入)到100mL水中,假设溶液体积变化不计,水溶液的导电能力最强的是( )
| A、HF |
| B、NH4HCO3 |
| C、BaSO4 |
| D、NH3 |
考点:电解质溶液的导电性,水的电离
专题:电离平衡与溶液的pH专题
分析:A.HF是弱电解质,在水中部分电离;
B NH4HCO3是强电解质,在水中完全电离;
C.BaSO4难溶于水;
D.NH3溶于水,生成的NH3?H2O,NH3?H2O是弱电解质,在水中部分电离.
B NH4HCO3是强电解质,在水中完全电离;
C.BaSO4难溶于水;
D.NH3溶于水,生成的NH3?H2O,NH3?H2O是弱电解质,在水中部分电离.
解答:
解:A.HF是弱电解质,在水中部分电离,导电能力不强;
B NH4HCO3是强电解质,在水中完全电离,电离出NH4+和HCO3-,导电能力比较强;
C.BaSO4不溶于水,导电能力很弱;
D.NH3溶于水,生成的NH3?H2O,NH3?H2O是弱电解质,在水中部分电离,导电能力也不强,
故水溶液的导电能力最强的是:NH4HCO3,
故选B.
B NH4HCO3是强电解质,在水中完全电离,电离出NH4+和HCO3-,导电能力比较强;
C.BaSO4不溶于水,导电能力很弱;
D.NH3溶于水,生成的NH3?H2O,NH3?H2O是弱电解质,在水中部分电离,导电能力也不强,
故水溶液的导电能力最强的是:NH4HCO3,
故选B.
点评:本题考查溶液的导电性,难度不大.要注意在相同条件下,可溶性的强电解质的水溶液的导电性比较强.

练习册系列答案
相关题目
下列物质既能发生消去反应,又能氧化成醛的是( )
| A、苯甲醇 |
| B、2,2-二甲基-1-丙醇 |
| C、2-甲基-1-丁醇 |
| D、甲醇 |
设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A、标准状况下,0.1mol Cl2溶于水,转移的电子数目为0.1NA |
| B、50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA |
| C、7.80g Na2O2与5.85g NaCl所含阴离子数相等 |
| D、常温常压下,18g H2O含有的中子数为10NA |
下列说法正确的是( )
A、按系统命名法,化合物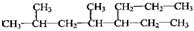 的名称为2,4-二甲基-5-丙基庚烷 的名称为2,4-二甲基-5-丙基庚烷 |
| B、人们生活中经常接触的聚乙烯、聚氯乙烯、聚苯乙烯、ABS工程塑料、顺丁橡胶等制品都是通过加聚反应得到的 |
| C、若两种二肽互为同分异构体,则二者的水解产物一定不相同 |
| D、分子式为C4H8Br2的有机物,结构中只含一个甲基的同分异构体(不考虑立体异构)有5种 |
反应NH4HS(s)?NH3(g)+H2S(g)在某一温度下达到平衡,下列各种情况中,能使化学平衡发生移动的是( )
| A、减少部分NH4HS固体 |
| B、压强、温度不变,充入少量氩气 |
| C、容积、温度一定,充入氦气 |
| D、温度、容积一定,充入SO2气体 |
下列说法不正确的是( )
| A、在高温条件下,C能置换出SiO2中的Si,说明C的非金属性比Si强 |
| B、单质硅是将太阳能转化为电能的常用材料 |
| C、熔融烧碱不能使用石英坩埚和陶瓷坩埚 |
| D、置换反应一定是氧化还原反应,不一定是离子反应 |
短周期非金属元素甲~戊在元素周期表中的相对位置如表所示,下面判断正确的是( )
| 甲 | 乙 | |
| 丙 | 丁 | 戊 |
| A、原子半径:甲<乙 |
| B、非金属性:乙<丁 |
| C、最高价氧化物的水化物的酸性:丙<丁 |
| D、最外层电子数:丙>丁>戊 |
对于合成氨反应:3H2(g)+N2(g)?2NH3(g)△H<0的四个图示,描述不正确的是( )
A、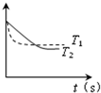 恒容条件下,已知该图中温度T1>T2,则纵轴可表示正反应速率 |
B、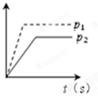 恒温下,已知该图中压强p1>p2,则纵轴可表示NH3的体积分数 |
C、 恒温、恒容下,该图中虚线表示开始充入2mol N2和3mol H2,实线表示开始充入1mol N2和3mol H2,则纵轴可表示H2的转化率 |
D、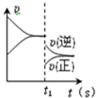 该图可表示平衡后,t1时在恒温恒压下充入He气时正、逆反应速率的变化曲线 |