题目内容
a mol FeS与b mol FeO投入到VL、c mol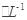 的硝酸溶液中充分反应,产生NO气体,所得澄清溶液成分可看作是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为( )
的硝酸溶液中充分反应,产生NO气体,所得澄清溶液成分可看作是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为( )
①(a+b)x63g ②(a+b)x189g ③(a+b)mol ④(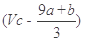 )mol
)mol
| A.①④ | B.②③ | C.①③ | D.②④ |
D
解析试题分析:第一种情况:硝酸有剩余。由电子守恒知:a mol FeS与b mol FeO:→Fe(NO3)3和H2SO4,共转移的电子的物质的量 (9a+b) mol,所以被还原的硝酸是(9a+b)/3 mol,则未被还原的硝酸为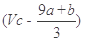 mol;第二种情况:硝酸恰好完全反应生成NO和Fe(NO3)3,则未被还原的硝酸的物质的量是3(a+b) mol,质量(a+b)x189g。所以D正确。
mol;第二种情况:硝酸恰好完全反应生成NO和Fe(NO3)3,则未被还原的硝酸的物质的量是3(a+b) mol,质量(a+b)x189g。所以D正确。
考点:氧化还原反应的计算方法。

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案向CuSO4溶液中逐滴加入过量KI溶液,观察到产生白色沉淀,溶液变为棕色。淀粉KI溶液中通入SO2气体,溶液无明显变化。则下列分析中正确的是
| A.白色沉淀是CuI2,棕色溶液含有I2 |
| B.滴加KI溶液时,转移2mol e- 时生成1mol白色沉淀 |
| C.通入SO2时,SO2与I—反应,I—作还原剂 |
| D.上述实验条件下,物质的氧化性:Cu2+>I2>SO2 |
有一未完成的离子方程式____+XO3-+6H+=3X2+3H2O,据此判断,氧化产物和还原产物的物 质的量之比为
| A.1∶1 | B.3∶1 | C.5∶1 | D.7∶1 |
在空气中,有下列反应发生:①N2+O2=2NO;②2NO+O2=2NO2;③3NO2+H2O=2HNO3+NO;④2SO2+O2=2SO3;⑤SO3+H2O=H2SO4;⑥SO2+H2O=H2SO3;⑦3O2=2O3。其中属于氧化还原反应的是( )
| A.①②③④ | B.①②③④⑦ | C.①②④⑦ | D.①②③④⑤⑥⑦ |
在xR2++yH++O2= mR3++nH2O的离子方程式中,对系数m和R3+的判断正确的是( )
| A.m="4" R2+是氧化产物 | B.m="y" R3+是氧化产物 |
| C.m="2" R3+是还原产物 | D.m="y" R3+是还原产物 |
高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂。下列反应可制取K2FeO4:
2Fe(OH)3+3Cl2+10KOH2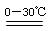 K2FeO4+KCl+8H2O
K2FeO4+KCl+8H2O
对于该反应,下列说法正确的是
| A.该反应是置换反应 | B.钾元素化合价降低 |
| C.Fe(OH)3发生还原反应 | D.Cl2是氧化剂 |
某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定ClO-与ClO3-的浓度之比为1∶3,则与溶液反应时被还原的氯元素与被氧化的氯元素的物质的量之比为( )
| A.21∶5 | B.11∶3 | C.4∶1 | D.3∶1 |
下列说法正确的是
| A.氧化还原反应的本质是有化合价的变化 |
| B.分解反应一定是氧化还原反应 |
| C.利用化合反应可制备FeCl2、Fe(OH)3 |
| D.在一定条件下能向正反两个方向进行的反应称为可逆反应 |