题目内容
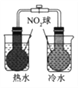
【题目】下图所示的实验,不能达到实验目的的是
A | B | C | D |
|
|
|
|
结合秒表测量锌与硫酸的反应速率 | 验证温度对化学平衡移动的影响 | 探究精炼铜的原理 | 证明酸性 CH3COOH>H2CO3>H3BO3 |
A. A B. B C. C D. D
【答案】C
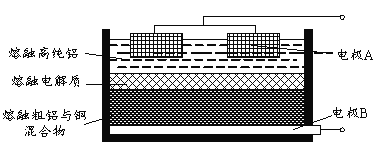
【解析】A.锌和硫酸反应生成氢气,根据收集一定体积的氢气所需时间,可测定消耗的硫酸的物质的量,根据浓度变化可计算反应速率,选项A正确;B.已知2NO2N2O4 △H<0,根据颜色的变化可知平衡移动的方向,以此可确定温度对平衡移动的影响,选项B正确;C、探究精炼铜的原理时应该将纯铜连接负极做为阴极,粗铜连接正极做为阳极,选项C错误;D、根据实验现象往硼酸中滴入碳酸钠溶液时不产生气泡,往醋酸中滴入碳酸钠时产生气泡可证明酸性:CH3COOH>H2CO3>H3BO3,选项D正确。答案选C。

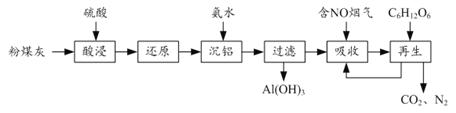
【题目】五氯化磷(PCl5)是有机合成中重要的氯化剂,易发生PCl5(s)![]() PCl3(g)+Cl2(g)反应。温度为T时,向2.0 L恒容密闭容器中充入1.0 mol PCl5,经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
PCl3(g)+Cl2(g)反应。温度为T时,向2.0 L恒容密闭容器中充入1.0 mol PCl5,经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
下列说法正确的是
A. 相同条件下,起始时向容器中充入2.0 mol PCl5,PCl5的分解率增大
B. 只升高温度,平衡时c(PCl5)=0.12 mol/L,则正反应是放热反应
C. 反应在前50 s的平均速率v(PCl3)=0.0032 mol/(L·s)
D. 在密闭低温的条件下,有利于PCl5固体的保存
【题目】用下图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是
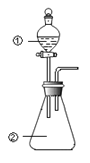
选项 | ①中物质 | ②中物质 | 预测②中的现象 |
A | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 立即产生气泡 |
B | 氯化铝溶液 | 浓氢氧化钠溶液 | 产生大量白色沉淀 |
C | 氯化铁溶液 | 淀粉碘化钾溶液 | 溶液变为蓝色 |
D | 硫酸亚铁溶液 | 过氧化钠固体 | 产生气泡和白色沉淀 |
A. A B. B C. C D. D