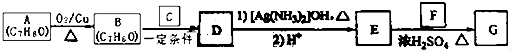题目内容
【题目】下列浓度关系正确的是( )
A. 0.1mol/L的NH4HSO4溶液中滴加0.1mol/L的Ba(OH)2溶液至沉淀刚好完全:c(NH4+)>c(OH-)>c(SO42-)>c(H+)
B. 若将CO2通入0.1mol/LNa2CO3溶液至溶液中性,则溶液中: 2c(CO32-)+c(HCO3-)=0.1mol/L
C. 0.1mol/L的NaOH溶液与0.2mol/L的HCN溶液等体积混合,所得溶液呈碱性:c(Na+)>c(CN-)>c(HCN)>c(OH-)>c(H+)
D. 向1L 1mol/L的KOH热溶液中通入一定量的Cl2,恰好完全反应生成氯酸钾、次氯酸钾和氯化钾的混合溶液:c(K+)+c(H+)=6c(ClO3-)+2c(ClO-)+c(HClO)+c(OH-)
【答案】D
【解析】A项,向0.1 mol/L的NH4HSO4溶液中滴加0.1 mol/L的Ba(OH)2溶液至沉淀刚好完全时发生反应为:NH4HSO4+Ba(OH)2=BaSO4↓+NH3H2O+H2O,电离方程式为:NH3H2O![]() NH4++OH-,H2O
NH4++OH-,H2O![]() H++OH-,所以c(OH-)应大于c(NH4+),故A错误;B项,将CO2通入0.1mol/LNa2CO3溶液至溶液中性,根据电荷守恒:2c(CO32-)+c(HCO3-)+c(OH-)=c(Na+)+c(H+),c(OH-)=c(H+),则2c(CO32-)+c(HCO3-)=c(Na+),又因为c(Na+)=0.2mol/L,所以2c(CO32-)+c(HCO3-)=0.2mol/L,故B错误;C项,0.1mol/L的NaOH溶液与0.2mol/L的HCN溶液等体积混合,发生反应:NaOH+HCN=NaCN+H2O,反应后溶液为NaCN和HCN等物质的量的混合溶液,因为所得溶液呈碱性,说明CN-的水解程度大于HCN的电离程度,所以各微粒的大小关系为:c(HCN)>c(Na+)>c(CN-)>c(OH-)>c(H+),故C错误;D项,由已知反应为:4Cl2+8KOH=6KCl+KClO+KClO3+4H2O,溶液中电荷守恒为:c(K+)+c(H+)=c(Cl-)+c(ClO3-)+c(ClO-)+c(OH-),氧化还原反应得失电子守恒为:c(Cl-)=5c(ClO3-)+c(ClO-)+c(HClO),将电子守恒等式代入上式得,c(K+)+c(H+)=6c(ClO3-)+2c(ClO-)+c(HClO)+c(OH-),故D正确。
H++OH-,所以c(OH-)应大于c(NH4+),故A错误;B项,将CO2通入0.1mol/LNa2CO3溶液至溶液中性,根据电荷守恒:2c(CO32-)+c(HCO3-)+c(OH-)=c(Na+)+c(H+),c(OH-)=c(H+),则2c(CO32-)+c(HCO3-)=c(Na+),又因为c(Na+)=0.2mol/L,所以2c(CO32-)+c(HCO3-)=0.2mol/L,故B错误;C项,0.1mol/L的NaOH溶液与0.2mol/L的HCN溶液等体积混合,发生反应:NaOH+HCN=NaCN+H2O,反应后溶液为NaCN和HCN等物质的量的混合溶液,因为所得溶液呈碱性,说明CN-的水解程度大于HCN的电离程度,所以各微粒的大小关系为:c(HCN)>c(Na+)>c(CN-)>c(OH-)>c(H+),故C错误;D项,由已知反应为:4Cl2+8KOH=6KCl+KClO+KClO3+4H2O,溶液中电荷守恒为:c(K+)+c(H+)=c(Cl-)+c(ClO3-)+c(ClO-)+c(OH-),氧化还原反应得失电子守恒为:c(Cl-)=5c(ClO3-)+c(ClO-)+c(HClO),将电子守恒等式代入上式得,c(K+)+c(H+)=6c(ClO3-)+2c(ClO-)+c(HClO)+c(OH-),故D正确。

 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案【题目】在一体积为10L的容器中,通入一定量的CO和H2O(g),在850℃时发生如下反应:CO(g)+H2O(g)CO2(g)+H2(g).CO和H2O(g)浓度变化如图 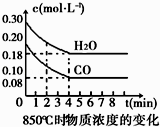
(1)0~4min的平均反应速率v(CO)=molL﹣1min﹣1 .
(2)该条件下,此反应的平衡常数K=(写表达式).
(3)该反应平衡时CO的转化率为 .
(4)能判断该反应达到化学平衡状态的依据是 . A.容器中压强不变 B.混合气体中c(CO)不变
C.v(H2)正=v(H2O)逆 D.c(CO2)=c(CO)
若降低温度,该反应的K值将 , 该反应的化学反应速率将(填“增大”“减小”或“不变”).
(5)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如表.
时间(min) | CO | H2O | CO2 | H2 |
0 | 0.200 | 0.300 | 0 | 0 |
2 | 0.138 | 0.238 | 0.062 | 0J062 |
3 | c1 | c2 | c3 | c3 |
4 | c1 | c2 | c3 | c3 |
5 | 0.116 | 0216 | 0.084 | |
6 | 0.096 | 0.266 | 0.104 |
①c1数值0.08molL﹣1(填大于、小于或等于).
②反应在4min~5min间,平衡向逆方向移动,可能的原因是 , 表中5min~6min之间数值发生变化,可能的原因是 .
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度.