题目内容
【题目】(1)已知Al(OH)3是两性氢氧化物,但不溶于弱碱溶液氨水,也不溶于弱酸碳酸。试用离子方程式说明原理:_____、_____。
(2)分子(CN)2中键与键之间的夹角为180°,并有对称性,分子中每个原子均满足8电子稳定结构。写出(CN)2的电子式_____。
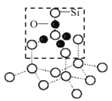
(3)请在下图的虚线框中补充完成SiO2晶体的结构模型示意图____,(部分原子已画出),并进行必要的标注。

【答案】![]() +
+![]() +2H2O=Al(OH)3↓+NH3H2O Al3++3
+2H2O=Al(OH)3↓+NH3H2O Al3++3![]() =Al(OH)3↓+3CO2↑或 2Al3++3
=Al(OH)3↓+3CO2↑或 2Al3++3![]() +3H2O=2Al(OH) 3↓+3CO2↑
+3H2O=2Al(OH) 3↓+3CO2↑ ![]()
【解析】
(1)偏铝酸钠和氯化铵发生双水解反应生成氢氧化铝和氨水,证明氢氧化铝不溶于氨水,反应的离子方程式是![]() +
+![]() + 2H2O=Al(OH)3↓+NH3H2O;氯化铝和碳酸氢钠溶液反应生成氢氧化铝沉淀和二氧化碳,证明氢氧化铝不溶于碳酸,反应的离子方程式是Al3++3
+ 2H2O=Al(OH)3↓+NH3H2O;氯化铝和碳酸氢钠溶液反应生成氢氧化铝沉淀和二氧化碳,证明氢氧化铝不溶于碳酸,反应的离子方程式是Al3++3![]() =Al(OH)3↓+3CO2↑;
=Al(OH)3↓+3CO2↑;
(2) (CN)2分子中每个原子均满足8电子稳定结构,(CN)2的电子式是![]() ;
;
(3) SiO2晶体中1个硅原子和4个氧原子形成4个硅氧单键,每个氧原子和2个硅原子形成2个氧硅单键,SiO2晶体的结构模型示意图为 。
。

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目